题目内容
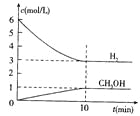
【题目】水煤气(CO和H2)是合成甲醇的重要原料,它可用水蒸气通过炽热的炭层制得:C(s)+H2O(g)![]() CO(g)+H2(g) ΔH=+131.3 kJ·mol-1
CO(g)+H2(g) ΔH=+131.3 kJ·mol-1
(1)该反应的平衡常数的表达式为_________________;升高温度,K值将________;容器中气体的平均相对分子质量将________。(填“增大”、“减小”或“不变”)。
(2)上述反应达到平衡后,将体系中的C(s)部分移走,平衡将________(填字母)。
A.向左移 B.向右移 C.不移动
(3)下列事实能说明该反应在一定条件下已达到平衡状态的有________(填字母)。
A.单位体积内每消耗1 mol CO的同时生成1 mol H2
B.混合气体总物质的量保持不变
C.生成H2O(g)的速率与消耗CO的速率相等
D.H2O(g)、CO、H2的浓度相等
(4)某温度下,将4.0 mol H2O(g)和足量的炭充入2 L的密闭容器中,发生如下反应,C(s)+H2O(g)![]() CO(g)+H2(g),达到平衡时测得K=1,则此温度下H2O(g)的转化率为________。
CO(g)+H2(g),达到平衡时测得K=1,则此温度下H2O(g)的转化率为________。
【答案】K=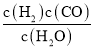 增大 减小 C AB 50%
增大 减小 C AB 50%
【解析】
(1)根据化学平衡常数的概念以及温度对化学平衡、化学平衡常数的影响分析;
(2)固体的浓度为常数,平衡不移动;
(3)依据平衡标志是正逆反应速率相同,各组分含量保持不变,结合反应特征和平衡移动原理分析选项;
(4)依据化学平衡三段式列式计算,转化率=![]() ×100%计算得到。
×100%计算得到。
(1)根据化学平衡常数为平衡时生成物浓度幂之积比反应物浓度幂之积,反应C(s)+H2O(g)![]() CO(g)+H2(g)的平衡常数的表达式为K=
CO(g)+H2(g)的平衡常数的表达式为K=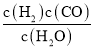 ;化学平衡常数的大小只与温度有关,升高温度,平衡向吸热的方向移动,反应C(s)+H2O(g)
;化学平衡常数的大小只与温度有关,升高温度,平衡向吸热的方向移动,反应C(s)+H2O(g)![]() CO(g)+H2(g) ΔH=+131.3 kJ·mol-1为吸热反应,升高温度,平衡正向移动,化学平衡常数增大;如果反应物完全转化为生成物,则容器中气体的平均相对分子质量是(28+2)/2=15,由于升高温度平衡向正反应方向进行,所以容器中气体的平均相对分子质量将减小。
CO(g)+H2(g) ΔH=+131.3 kJ·mol-1为吸热反应,升高温度,平衡正向移动,化学平衡常数增大;如果反应物完全转化为生成物,则容器中气体的平均相对分子质量是(28+2)/2=15,由于升高温度平衡向正反应方向进行,所以容器中气体的平均相对分子质量将减小。
(2)上述反应达到平衡后,将体系中的C(s)部分移走,浓度不变,平衡不移动;
答案选C;
(3)A.单位体积内每消耗1mol CO的同时生成1molH2,说明一氧化碳或氢气正逆反应速率相同,反应达到平衡状态,选项A正确;
B.反应前后气体物质的量变化,混合气体总物质的量保持不变说明反应达到平衡状态,选项B正确;
C.生成H2O(g)的速率与消耗CO的速率相等只能说明反应逆向进行,不能说明反应达到平衡状态,选项C错误;
D.H2O(g)、CO、H2的浓度相等和起始量变化量有关,不能作为平衡标志,选项D错误;
答案选AB;
(4)设H2O转化了xmol/L,依据化学平衡三段式列式计算:
C(s)+H2O(g)![]() CO(g)+H2(g)
CO(g)+H2(g)
初始浓度(mol/L) 2.0 0 0
转化浓度(mol/L) x x x
平衡浓度(mol/L) 2.0-x x x
达到平衡时测得K=1,即K=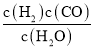 =
=![]() =1,解得x=1mol/L,所以α(H2O)=
=1,解得x=1mol/L,所以α(H2O)=![]() ×100%=50%。
×100%=50%。

 阅读快车系列答案
阅读快车系列答案【题目】下列有关实验现象和解释或结论都正确的是
选项 | 实验操作 | 现象 | 解释或结论 |
A | 向淀粉的酸性水解液中滴入少量新制Cu(OH)2悬浊液并加热 | 有砖红色沉淀生成 | 葡萄糖具有还原性 |
B | NaAlO2溶液与NaHCO3溶液混合 | 白色絮状沉淀生成 | 二者水解相互促进生成氢氧化铝沉淀 |
C | 将充满NO2的密闭玻璃球浸泡在热水中 | 红棕色变深 | 反应2NO2 的△H<0 |
D | 向盛有1mL0.l mol/L的AgNO3溶液中加入10滴0.1mol/L的NaCl溶液,振荡,再加入10滴0.1mol/L的NaI溶液,再振荡 | 先生成白色沉淀,后产生黄色沉淀 | Ksp(AgI)sp(AgCl) |
A. A B. B C. C D. D