��Ŀ����
����Ŀ�����Ȼ����Ǻϳ��������ε���Ҫԭ�ϣ������ϳɺ��л��ϳ�������Ҫ�����ã��Ǻϳ��������Ӽ�����Ҫ�ɷݣ���ҵ����Ҫ����ýȾ����������������ˮ�������Ҵ����������������ѣ��׳��⣬���������ڸ������ܱ����������������������ܱ�H2O2����ΪCr��������2CrO42��+2H+Cr2O72��+H2O�������Ȼ������������£�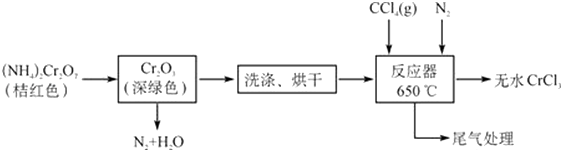
��1�����Ȼ������������±�H2O2����ΪCr�����������ӷ�Ӧ����ʽΪ ��
��2����֪CCl4�е�Ϊ57.6�棬Ϊ��֤�ȶ���CCl4���������˵ļ��ȷ�ʽ�� ��
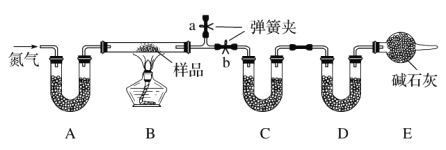
��3������ͼװ���Ʊ�CrCl3ʱ����Ҫ���������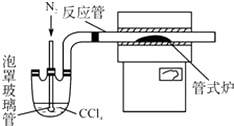
�ٽ������ռ����������У��ڼ��ȷ�Ӧ����400�棬��ʼ��������ƿ��ͨ�뵪�����������µ�650�棻��������ƿ��װ��150mLCCl4 �� ������CCl4 �� �¶ȿ�����50��60��֮�䣻�ܷ�Ӧ�ܳ��ڶ˳�����CrCl3������ʱ���жϼ��ȹ�ʽ¯�ĵ�Դ����ֹͣ����CCl4 �� ����ͨ�뵪�������װ�������ԣ�
��ȷ�IJ���˳��Ϊ���ޡ��ۡ� �� �������ͨ�絪�������� ��
��4����֪��Ӧ���з�������Ҫ��Ӧ�У�Cr2O3+3CCl4��2CrCl3+3COCl2 �� ������綾��ʵ������ͨ����н��У������Ҵ�����COCl2 �� ����һ�ֺ���������C5H10O3�������Ҵ�����β���Ļ�ѧ����ʽ ��
��5����Ʒ�����Ȼ������������IJⶨ��ȡ��Ʒ0.3300g����ˮ�ܽⲢ������250mL����ƿ�У���ȡ25.00mL�ڵ���ƿ��һ�ִ�������ƿ���У��������к����1gNa2O2 �� ��ּ�����У��ʵ�ϡ�ͣ�Ȼ����������2mol/LH2SO4����Һ��ǿ���ԣ���ʱ����Cr2O72�����ڣ��ټ���1.1gKI��������ҡ�ȣ��ڰ�������5���Ӻ���1mLָʾ������0.0250mol/L�����������Һ�ζ����յ㣬ƽ�вⶨ���Σ�ƽ�����ı������������Һ24.00mL����֪��Cr2O72��+6I��+14H+=2Cr3++3I2+7H2O��2Na2S2O3+I2�TNa2S4O6+2NaI��
��ָʾ��Ϊ �� �ζ��յ������Ϊ ��
���������ƿ��CrCl3��Һ�������У�����Na2O2��ҲҪ������У�����Ҫԭ���� ��
����Ʒ����ˮ���Ȼ�������������Ϊ �� ����������ȷ��0.1%��
���𰸡�
��1��2Cr3++3H2O2+10OH��=2CrO ![]() +8H2O
+8H2O
��2��ˮԡ���ȣ������¶ȼ�ָʾ�¶ȣ�
��3���ڡ��ܡ��ݡ���CCl4���������뷴Ӧװ���У����߿�������ֹCrCl3������
��4��COCl2+2C2H5OH��C2H5OCOC2H5+2HCl
��5�����ۣ����һ�ε���ʱ����ɫǡ����ȫ��ȥ���Ұ�����ڲ��ָ�ԭɫ����ȥ�����ܽ����������ֹ������I������������ƫ�ߵ���96.1%
���������⣺��1�����Ȼ������������±�H2O2����Ϊ����������ݵ���غ��Ԫ���غ��֪���ӷ���ʽΪ2Cr3++3H2O2+10OH��=2CrO42��+8H2O�����Դ��ǣ�2Cr3++3H2O2+10OH��=2CrO42��+8H2O����2����ΪCCl4�е�Ϊ76.8�棬�¶ȱȽϵͣ���˱�֤�ȶ���CCl4����������ͨ��ˮԡ�����������������������¶ȼ�ָʾ�¶ȣ����Դ��ǣ�ˮԡ���ȣ������¶ȼ�ָʾ�¶ȣ�����3���ɣ�4����֪��Ӧ�Ʊ�ԭ��ΪCr2O3+3CCl4��2CrCl3+3COCl2 �� ���Ȼ�̼�ڹ�ʽ¯�з�Ӧ����Cr2O3��Ӧ����Ӧ�ܳ��ڶ˳�����CrCl3������ʱ���жϼ��ȹ�ʽ¯�ĵ�Դ��ֹͣ����CCl4 �� ����ͨ�뵪�����������ռ��������ʲ���˳��Ϊ���ޡ��ۡ��ڡ��ܡ��ݡ��٣��������ͨ�뵪�������Խ�CCl4�������뷴Ӧװ���У����߿�������ֹCrCl3�����������Դ��ǣ��ڡ��ܡ��ݡ��٣���CCl4�������뷴Ӧװ���У����߿�������ֹCrCl3����������4���ɷ���ʽ��֪��COCl2�е�2��Clԭ�ӱ�2����OC2H5���棬���Ҵ���COCl2����ȡ����Ӧ����OC2H5ȡ����ԭ������C2H5OCOC2H5��HCl����Ӧ����ʽΪCOCl2+2C2H5OH��C2H5OCOC2H5+2HCl�����Դ��ǣ�COCl2+2C2H5OH��C2H5OCOC2H5+2HCl����5��������Na2S2O3�ζ�����I2 �� I2����������ɫ�����Կ����õ�����ָʾ�����������һ��ʱ�������Һ��ɫ�ڰ�����ڲ���ɫ����ﵽ�ζ��յ㣬���Դ��ǣ����ۣ����һ�ε���ʱ����ɫǡ����ȫ��ȥ���Ұ�����ڲ��ָ�ԭɫ������Һ�����ܽ��������������������I��������������ȥ�����ܽ������ʹ���ɵ�I2����������ƫ�ߵ����ʼ�����У�����Ҫԭ���ǣ���ȥ�����ܽ����������ֹ������I������������ƫ�ߵ������Դ��ǣ���ȥ�����ܽ����������ֹ������I������������ƫ�ߵ�������25.00mL��Һ��n��Cr3+������CrԪ���غ㼰����ʽ�ɵù�ϵʽ2Cr3++��Cr2O72����3I2��6Na2S2O3 �� ���ݹ�ϵʽ���㣬
2Cr3++��Cr2O72����3I2��6Na2S2O3 ��
2 6
n��Cr3+�� 0.0250mol/L��0.024L
��n��Cr3+��=0.0250mol/L��0.024L�� ![]() ������250mL��Һ��n�䣨Cr3+��=0.0250mol/L��0.024L��
������250mL��Һ��n�䣨Cr3+��=0.0250mol/L��0.024L�� ![]() ��
�� ![]() =0.002mol������CrԪ���غ��֪n��CrCl3��=n�䣨Cr3+��=0.002mol��������Ʒ��m��CrCl3��=0.002mol��158.5g/mol=0.317g������Ʒ����ˮ���Ȼ�������������Ϊ
=0.002mol������CrԪ���غ��֪n��CrCl3��=n�䣨Cr3+��=0.002mol��������Ʒ��m��CrCl3��=0.002mol��158.5g/mol=0.317g������Ʒ����ˮ���Ȼ�������������Ϊ ![]() ��100%=96.1%��
��100%=96.1%��
���Դ��ǣ�96.1%��