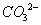题目内容
室温下,下列各组离子在指定溶液中一定能大量共存的是
| A.pH=1的溶液中:Fe3+、NO3-、Cl-、Na+ |
| B.由水电离的c(H+)=10-12mol·L-1的溶液中:Cl-、CO32-、K+、SO32- |
| C.c(OH-)/c(H+)=1012的溶液中:SO32-、NH4+、NO3-、K+ |
| D.能使甲基橙呈红色的溶液中:Na+、AlO2-、NO3-、HCO3- |
A
试题分析:pH=1的溶液为强酸性溶液,Fe3+、NO3-、Cl-、Na+这四种离子都可以大量共存,故A正确,为本题的答案;由水电离的c(H+)=10-12mol·L-1的溶液可以是强酸性溶液,也可以是强碱性溶液,若溶液为强酸性溶液,则CO32-、SO32-都不可以大量共存,故B不正确;c(OH-)/c(H+)=1012的溶液为强碱性溶液,NH4+不能再强碱性溶液中大量共存,故C错误;能使甲基橙呈红色的溶液中为酸性溶液,AlO2-、HCO3-不能在酸性溶液中大量共存,故D不正确。
点评:本题考查了离子共存的问题,离子共存问题是高考考查的重点和难点,该题综合性好,有一定的难度,注意的是由水电离的c(H+)=10-12mol·L-1的溶液可以是酸性溶液,也可以是碱性溶液。

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
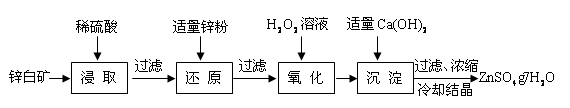

 ,该溶液中:
,该溶液中: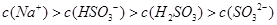
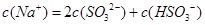
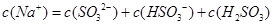
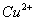 、
、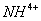 、
、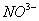 、
、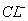
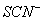 、
、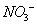 、
、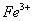 、
、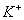
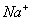 、
、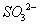
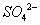 、
、 、
、