题目内容
【题目】下表列出了①~⑨九种元素在周期表中的位置:
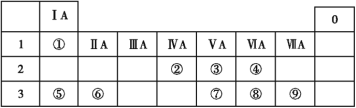
请按要求回答下列问题。
(1)元素③的名称是__,元素⑨的元素符号是____,元素④形成的单质具有____(填“氧化性”或“还原性”)。
(2)元素⑦⑧⑨的气态氢化物的稳定性由弱到强的顺序:____(用化学式表示)。
(3)写出一条能说明元素⑤的金属性比元素⑥强的事实:_____。
(4)写出元素⑤形成的单质与水反应的离子方程式:_____。
【答案】氮 Cl 氧化性 PH3<H2S<HCl 钠能与冷水剧烈反应产生氢气,镁与冷水反应缓慢或与沸水反应迅速[或碱性:NaOH>Mg(OH)2] 2Na+2H2O=2Na++2OH-+H2↑
【解析】
根据①~⑨九种元素在周期表中的位置,①是H元素;②是C元素;③是N元素;④是O元素;⑤是Na元素;⑥是Mg元素;⑦是P元素;⑧是S元素;⑨是Cl元素。
(1)元素③是N元素,名称是氮;⑨的元素符号是Cl;④是O元素,最外层有6个电子,易得电子,形成的单质氧气,具有氧化性;
(2)同周期元素从左到右非金属性增强,非金属性越强气态氢化物越稳定,元素P、S、Cl的气态氢化物的稳定性由弱到强的顺序是PH3<H2S<HCl;
(3)金属性越强越易与水反应,钠能与冷水剧烈反应产生氢气,镁与冷水反应缓慢,说明Na的金属性比Mg强;或碱性:氢氧化钠大于氢氧化镁,也可证明;
(4)钠与水反应生成氢氧化钠和氢气,反应的离子方程式是2Na+2H2O=2Na++2OH-+H2↑。

【题目】类比推理是学习化学的重要的思维方法,下列陈述Ⅰ及类比推理陈述Ⅱ均正确的是( )
陈述Ⅰ | 类比推理陈述Ⅱ | |
A | 单质的熔点Br2 < I2 | 单质的熔点Li < Na |
B | 工业上电解熔融的Al2O3得到铝单质 | 工业上电解熔融的MgO得到镁单质 |
C | 还原性:I- > Br- | 还原性:P3- > N3- |
D | 溶解度:CaCO3<Ca(HCO3)2 | 溶解度:Na2CO3<NaHCO3 |
A.AB.BC.CD.D