题目内容
2.下列哪种方法可以制取镁( )| A. | MgO+Al | B. | 电解熔融的MgCl2 | C. | 加热MgCl2 | D. | MgO+C(高温) |
分析 A.铝的活泼性弱于镁;
B.电解氯化镁生成镁与氯气;
C.氯化镁非常稳定;
D.氧化镁与炭不反应.
解答 解:A.铝的活泼性弱于镁,氧化镁与铝不反应,故A不选;
B.电解氯化镁生成镁与氯气,能够制取镁,故B选;
C.氯化镁非常稳定,受热不分解,故C不选;
D.氧化镁与炭不反应,不能制取镁,故D不选;
故选:B.
点评 本题考查了金属的制备,熟悉不同金属制备原理、熟悉镁的性质是解题关键,题目不难.

练习册系列答案
 发散思维新课堂系列答案
发散思维新课堂系列答案
相关题目
10.将少量的金属钠投入到过量的AlCl3溶液中,产生的现象是( )
| A. | 只有气体产生 | B. | 生成白色沉淀 | ||
| C. | 生成无色透明溶液 | D. | 产生气体和白色沉淀 |
17.某溶液中含有大量的Cl-、CO32-、OH-,如果只取一次该溶液分别将三种离子检验出来,下列添加试剂的顺序正确的是( )
| A. | 先加Mg(NO3)2,再加Ca(NO3)2,最后加AgNO3 | |
| B. | 先加Ca(NO3)2,再加AgNO3,最后加Mg(NO3)2 | |
| C. | 先加AgNO3,再加Ca(NO3)2,最后加Mg(NO3)2 | |
| D. | 先加Ca(NO3)2,再加Mg(NO3)2,最后加AgNO3 |
7.现有铁和铜组成的合金共a mol,其中铜的物质的量分数为x.将此合金研成粉末状后全部投入含bmolHNO3的稀溶液中,微热使其充分反应,HNO3还原产物只得到NO.
(1)用粒子符号填写下列空白(列举出全部可能出现的情况).
(2)当溶液中金属离子只有Fe2+、Cu2+时,则b的取值范围是(用a,x表示)$\frac{8a(1-x)}{3}$<b≤$\frac{8a}{3}$.
(3)当x=0.5,溶液中Fe3+和Fe2+的物质的量相等时,在标准状况下共产生672mlNO气体.求a和b的值a=0.04mol,b=0.12mol.
(1)用粒子符号填写下列空白(列举出全部可能出现的情况).
| 组序 成分 | ① | ② | ③ | ④ | ⑤ | ⑥ |
| 残留固体成分 | ||||||
| 溶液中的金属离子 |
(3)当x=0.5,溶液中Fe3+和Fe2+的物质的量相等时,在标准状况下共产生672mlNO气体.求a和b的值a=0.04mol,b=0.12mol.
11.将某合金(仅含铜、铁)全部投入50mL b mol•L-1的硝酸溶液中,加热使其充分反应(假设NO是唯一的还原产物),下列说法正确的是( )
| A. | 若金属有剩余,在溶液中再滴入硫酸后,金属又开始溶解 | |
| B. | 若金属全部溶解,则溶液中一定含有Fe3+ | |
| C. | 若硝酸有剩余,溶液中可能含有Fe2+ | |
| D. | 若金属全部溶解,且产生336mL气体(标准状况下),则b=0.3 |
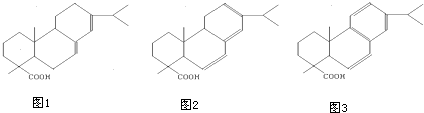
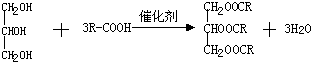 ;
;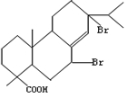 ;
;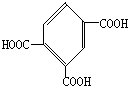 .
.