题目内容
2.下列溶液中,Na+的物质的量浓度最大的是( )| A. | 5 mL 0.6mol•L-1 Na2SO4溶液 | B. | 10 mL 0.3 mol•L-1 Na3PO4溶液 | ||
| C. | 5 mL 0.4 mol•L-1 NaOH溶液 | D. | 10mL 0.5 mol•L-1 NaNO3溶液 |
分析 钠离子的物质的量浓度与各溶液中溶质的物质的量浓度及溶质的化学式组成有关,与溶液的体积大小无关,据此对各选项进行计算与判断.
解答 解:A.5 mL 0.6mol•L-1 Na2SO4溶液中Na+的物质的量浓度为:0.6mol/L×2=1.2mol/L;
B.10 mL 0.3 mol•L-1 Na3PO4溶液中Na+的物质的量浓度为:0.3mol/L×3=0.9mol/L;
C.5 mL 0.4 mol•L-1 NaOH溶液中Na+的物质的量浓度为:0.4mol/L×1=0.4mol/L;
D.10mL0.5 mol•L-1 NaNO3溶液中Na+的物质的量浓度为:0.5mol/L×1=0.5mol/L;
根据分析可知,Na+的物质的量浓度最大的是A,
故选A.
点评 本题考查了物质的量浓度的计算,题目难度不大,明确物质的量浓度的含义为解答关键,注意物质的量浓度与溶液体积大小无关,为易错点,试题培养了学生的灵活应用能力.

练习册系列答案
相关题目
12.己知:2Fe+3Br2=2FeBr3,Fe2+的还原性大于Br-.现有16.8g铁和0.3mol Br2反应后加入水得到澄清溶液后,通入a mol Cl2.下列叙述不正确的是( )
| A. | 当a=0.1时,发生的反应为2Fe2++Cl2-2Fe3++2C1- | |
| B. | 当a=0.45时,发生的反应为2Fe2++4Br-+3Cl2=2Fe3++2Br2+6Cl- | |
| C. | 若溶液中Br-有一半被氧化时,c (Fe3+):c(Br-):c (Cl-)-1:1:3 | |
| D. | 当0<a<0.15时,溶液中始终满足2c(Fe2+)+3c (Fe3+)+c(H)=c(C1-)+c(Br-)+c(OH-) |
17.在容积固定的容器中发生反应:A(g)+2B(g)═C (g)△H<0,各物质浓度如表所示:
下列说法错误的是( )
| 浓度 时间 | c(A)/mol•L-1 | c(B)/mol•L-1 | c(C)/mol•L-1 |
| 0 | 0.8 | 1.6 | 0 |
| 2min | 0.6 | x | 0.2 |
| 4min | 0.3 | 0.6 | 0.5 |
| 6min | 0.3 | 0.6 | 0.5 |
| A. | 2~4 min内用B表示的平均反应速率为0.3 mol•L-1•min-1 | |
| B. | 反应在第2 min时改变了条件,可能是加入了催化剂 | |
| C. | 反应在第2 min时改变了条件,可能是增加了B的浓度 | |
| D. | 若加入催化剂,平衡时气体混合物的总物质的量保持不变 |
7.设NA表示阿伏德罗常数的值,下列叙述正确的是( )
| A. | 标准状况下,2.24LCH4含有的H原子数为0.1NA | |
| B. | 常温常压下,NA个CO2分子占有的体积为22.4L | |
| C. | 1 mol•L-1A1Cl3溶液中含有的Cl-数目为3NA | |
| D. | 2.4g金属镁变为镁离子时失去的电子数为0.2 NA |
11.把温度为20℃,浓度为1.0mol•L-1的H2SO4和2.2mol•L-1的碱溶液各50mL混合(溶液密度均为1g•mL-1,比热容为4.184kJ•K-1•kg-1)轻轻搅动,测得酸碱混合液的温度变化数据如下:
则反应NH3•H2O?NH${\;}_{4}^{+}$+OH-的焓变约为(单位:kJ•mol-1)( )
| 反应物 | 起始温度t1℃ | 终止温度t2℃ |
| H2SO4+NaOH | 20 | 33.6 |
| H2SO4+NH3•H2O | 20 | 32.6 |
| A. | 2.1 | B. | 4.2 | ||
| C. | 52.7 | D. | 缺少数据无法计算 |
3.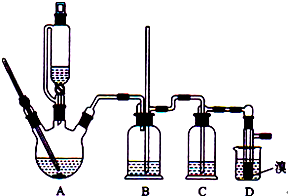 实验室制备1,2-二溴乙烷的反应原理如下:
实验室制备1,2-二溴乙烷的反应原理如下:
CH3CH2OH→CH2=CH2+H2O
CH2=CH2+Br2→BrCH2CH2Br
可能存在的副反应有:乙醇在浓硫酸的存在下l40℃脱水生成乙醚.用少量的溴和足量的乙醇制备1,2-二溴乙烷,装置如图所示:有关数据列表如下:
回答下列问题:
(1)在此制备实验中,要尽可能快地把反应温度升高到170℃左右,其目的有ad(填正确选项前的字母)
a.引发反应
b.加快反应速度
c.防止乙醇挥发
d.减少副产物乙醚生成
(2)将1,2-二溴乙烷粗产品置于分液漏斗中加水,振荡后静置,产物应在下层(填“上”、“下”)
(3)实验过程中装置B可以防止倒吸,并检查装置C、D是否堵塞,写出装置D堵塞时B中的现象当装置发生堵塞时,B装置中液体会压入的长玻璃导管,甚至溢出导管,以观测和缓解气压增大
(4)判断该制备反应已经结束的最简单方法是溴的颜色完全褪去
(5)反应过程中应用冷水冷却装置D,其主要目的是冷却可避免溴的大量挥发;但又不能过度冷却(如用冰水),其原因是产品1,2-二溴乙烷的熔点(凝固点)低,过度冷却会凝固而堵塞导管.
 实验室制备1,2-二溴乙烷的反应原理如下:
实验室制备1,2-二溴乙烷的反应原理如下:CH3CH2OH→CH2=CH2+H2O
CH2=CH2+Br2→BrCH2CH2Br
可能存在的副反应有:乙醇在浓硫酸的存在下l40℃脱水生成乙醚.用少量的溴和足量的乙醇制备1,2-二溴乙烷,装置如图所示:有关数据列表如下:
| 乙醇 | 1,2-二溴乙烷 | 乙醚 | |
| 状态 | 无色液体 | 无色液体 | 无色液体 |
| 密度/g•cm-3 | 0.79 | 2.2 | 0.71 |
| 沸点/℃ | 78.5 | 132 | 34.6 |
| 熔点/℃ | -130 | 9 | -116 |
(1)在此制备实验中,要尽可能快地把反应温度升高到170℃左右,其目的有ad(填正确选项前的字母)
a.引发反应
b.加快反应速度
c.防止乙醇挥发
d.减少副产物乙醚生成
(2)将1,2-二溴乙烷粗产品置于分液漏斗中加水,振荡后静置,产物应在下层(填“上”、“下”)
(3)实验过程中装置B可以防止倒吸,并检查装置C、D是否堵塞,写出装置D堵塞时B中的现象当装置发生堵塞时,B装置中液体会压入的长玻璃导管,甚至溢出导管,以观测和缓解气压增大
(4)判断该制备反应已经结束的最简单方法是溴的颜色完全褪去
(5)反应过程中应用冷水冷却装置D,其主要目的是冷却可避免溴的大量挥发;但又不能过度冷却(如用冰水),其原因是产品1,2-二溴乙烷的熔点(凝固点)低,过度冷却会凝固而堵塞导管.
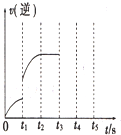 一定温度下体积为5L的密闭容器中发生可逆反应.
一定温度下体积为5L的密闭容器中发生可逆反应.
