题目内容
3.下列金属中用电解方法进行冶炼的是( )| A. | 铝 | B. | 铜 | C. | 银 | D. | 铁 |
分析 依据金属活泼性,一般活泼的金属用电解法,较活泼的金属用热还原法,不活泼的金属例如汞、银等用热分解法,据此解答
解答 解:A.铝性质活泼,用电解氧化铝方法冶炼,故A选;
B.Cu用热还原法冶炼,故B不选;
C.Ag用热分解法冶炼,故C不选;
D.Fe用热还原法冶炼,故D不选;
故选:A.
点评 本题考查金属冶炼的一般方法和原理,根据金属的活泼性采用相应的冶炼方法,难度不大,注意相关知识的积累.

练习册系列答案
 名校练考卷期末冲刺卷系列答案
名校练考卷期末冲刺卷系列答案
相关题目
13.下列对于有机物的结构简式、键线式书写错误的是( )
| A. | 丙炔:CH≡C-CH3 | |
| B. | 丙烯:CH2CHCH3 | |
| C. | 2丁烯的结构简式为CH3CH═CHCH3,其键线式为 | |
| D. | 乙醇:CH3CH2OH |
14.下列关于工业生产的说法正确的是( )
| A. | 工业生产中催化剂被大量使用是因为催化剂可以提高反应速率和转化率 | |
| B. | 合成氨的工业生产需在高温、高压和催化剂条件下进行是因为该反应是吸热反应 | |
| C. | 合成氨的工业生产中,及时将NH3液化分离出来将有利于提高生成物的产量 | |
| D. | 硫酸的工业生产中,SO2的催化氧化没有采用高压是因为压强对该反应无影响 |
18.已知混合烃的平均分子式为C1.5H4,则还混合烃中( )
| A. | 一定没有甲烷 | B. | 一定有乙烯 | C. | 一定有丙烷 | D. | 一定没有乙烷 |
8.下列表述正确的是( )
| A. | 某离子第三层上和第二层上的电子数均为第一层的4倍 | |
| B. | Cl-的结构示意图: | |
| C. | 某物质的焰色反应为黄色,某物质一定为钠的化合物 | |
| D. | 14C和14N的质量数相等,互称为同位素 |
15.下列实验方案,不能达到相应的实验目的是( )
| A | B | C | D | |
| 实验方案 | 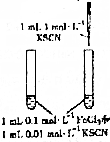 | 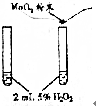 | 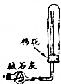 |  加热大试管,一段时间后,蒸发皿中产生肥皂泡,点燃 |
| 目的 | 探究反应物浓度对化学平衡的影响 | 证明MnO2作该反应的催化剂 | 干燥并收集氨气 | 探究铁与水蒸气能否反应 |
| A. | A | B. | B | C. | C | D. | D |
10.设反应①Fe(s)+CO2(g)?FeO(s)+CO(g)△H=Q1的平衡常数为K1,
反应②Fe(s)+H2O(g)?FeO(s)+H2(g)△H=Q2的平衡常数为K2,
反应③H2(g)+CO2(g)?CO(g)+H2O(g)△H=Q3,平衡常数为K3.
请结合表中在不同温度下K1、K2的值,回答下列问题:
(1)反应①的平衡常数表达式K1=$\frac{[CO]}{[C{O}_{2}]}$,△H>0(填“>”、“<”或“=”).
(2)根据反应①与②推导出Q1、Q2、Q3的关系式:Q3=Q3=Q1-Q2.计算出在1173K时反应③的平衡常数K3的数值:K3=1.4.
(3)能判断反应③已达到化学平衡状态的依据是CD.
A.容器中压强不变 B.△H不变 C.v正(H2)=v逆(CO) D.CO的质量分数不变.
反应②Fe(s)+H2O(g)?FeO(s)+H2(g)△H=Q2的平衡常数为K2,
反应③H2(g)+CO2(g)?CO(g)+H2O(g)△H=Q3,平衡常数为K3.
请结合表中在不同温度下K1、K2的值,回答下列问题:
| T/K | K1 | K2 |
| 973 | 1.47 | 2.38 |
| 1173 | 2.20 | 1.50 |
(2)根据反应①与②推导出Q1、Q2、Q3的关系式:Q3=Q3=Q1-Q2.计算出在1173K时反应③的平衡常数K3的数值:K3=1.4.
(3)能判断反应③已达到化学平衡状态的依据是CD.
A.容器中压强不变 B.△H不变 C.v正(H2)=v逆(CO) D.CO的质量分数不变.