题目内容
1.化学与环境、生活、材料密切相关,下列说法正确的是( )| A. | 安装煤炭燃烧过程的“固硫”装置,主要是为了提高煤的利用率 | |
| B. | 二氧化氯和三氯化铁都常用于自来水的处理,二者的作用原理是相同的 | |
| C. | 通过有机合成,可以制造出比钢铁更强韧的新型材料 | |
| D. | 气溶胶和液溶胶的差别在于分散质的物质状态 |
分析 A、安装煤炭燃烧过程的“固硫”装置,是为了减少硫的化合物的排放;
B、二氧化氯具有强氧化性,可杀菌消毒,三氯化铁水解生成具有吸附性的氢氧化铁,可除去水中的悬浮物;
C、某些新型高分子材料的性能比钢铁更强韧分析;
D、所谓溶胶就是胶体溶液,是由分散质的细小粒子分散在介质中形成的分散物系.溶胶的分类由分散介质来决定.
解答 解:A、安装煤炭燃烧过程的“固硫“装置,主要是为了减少二氧化硫的排放,避免形成酸雨防止污染空气,故A错误;
B、二氧化氯净水是利用其氧化性,三氯化铁净水是利用胶体的吸附性,二者的作用原理是不相同的,故B错误;
C、通过有机物的合成可以制造出新型高分子材料,某些新型高分子材料的性能比钢铁更强韧,故C正确;
D、所谓溶胶就是胶体溶液,是由分散质的细小粒子分散在介质中形成的分散物系.溶胶的分类由分散介质来决定(也就是溶液中的溶剂),如果是气态介质,就是气溶胶;液态介质,就是液溶胶;固态介质,就是固溶胶,故D错误;
故选C.
点评 本题考查了盐类水解分析,物质性质的理解应用,掌握基础是关键,题目难度中等.

练习册系列答案
 53随堂测系列答案
53随堂测系列答案
相关题目
12.在实验室里,下列除去杂质的方法正确的是 ( )
| A. | 溴苯中混有溴,加入KI溶液,用汽油萃取出溴 | |
| B. | 乙烷中混有乙烯,在一定条件下反应通入氢气,使乙烯转化为乙烷 | |
| C. | 硝基苯中混有浓硝酸和浓硫酸,将其倒入浓烧碱溶液中,静置,然后分液 | |
| D. | 乙烷中混有CO2,将其通入碳酸氢钠溶液洗气后干燥 |
9.25℃时,用Na2S沉淀Cu2+、Zn2+两种金属离子(M2+),所需S2-最低浓度的对数值lgc(S2-)与lgc(M2+)关系如图所示.下列说法正确的是( )
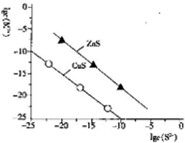

| A. | Na2S溶液中:c(S2-)+c(HS-)+c(H2S)=2c(Na+) | |
| B. | 25℃时K甲(CuS)均为1×10-28 | |
| C. | 向l00mLZn2+、Cu2+均为10-5mol•L-1 的混合溶液中逐滴加入10-4mol•L-1 Na2S溶液,Zn2+先沉淀 | |
| D. | 向Cu2+浓度为10-5mol•L-1工业废水中加入ZnS粉末,会有CuS沉淀析出 |
16.已知W、X、Y、Z为原子序数依次增大的短周期主族元素,X、Y、Z同周期,W、Z同主族,其中X、Y为金属元素,W与Y的原子序数相差5,下列说法正确的是( )
| A. | X离子的氧化性大于Y离子 | B. | W的气态氢化物的稳定性比Z的弱 | ||
| C. | 含Y的盐溶液一定显酸性 | D. | X离子的半径小于W离子 |
6.下列关于AlCl3的说法中正确的是( )
| A. | AlCl3溶液中还可能大量存在:H+、NH4+、SO42-、NO3- | |
| B. | AlCl3溶液与过量的氨水反应的离子方程式为:Al3++4NH3•H2O═4NH4++AlO2-+2H2O | |
| C. | 若NA为阿伏伽德罗常数的值,则1L0.1mol•L-1的AlCl3溶液中Al3+的数目为0.1NA | |
| D. | 工业上可用电解熔融的AlCl3来制取金属Al |
10.-种新型试剂常用于氧化降解溶液中的有机污染物(用X表 示),在一定条件下反应开始时其浓度为2.0×10-3mol•L-1,反应10 min后进行测定,测得数据如图1、图2所示,则下列有关说法正确的是( )
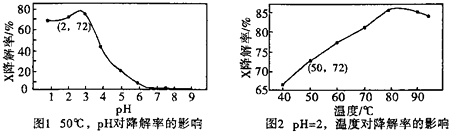

| A. | pH=2、温度为50℃、10 min时,X的物质的量浓度c( X)为5.6×10-4mol•L-1 | |
| B. | 图2说明:任何条件下X降解率均随温度升高先增后减 | |
| C. | 无需再进行后续实验,就可以判断最佳反应条件是:pH=3、温度为80℃ | |
| D. | 图1说明:50℃时,X的降解率随溶液PH的增大而逐渐减小 |
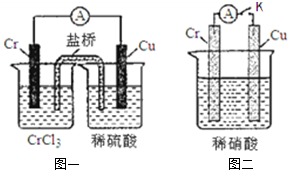 在如图装置中,观察到图一装置铜电极上产生大量的无色气泡.而在图二装置中当开关K断开时,铬电极无现象,K闭合时,铬电极上产生大量无色气体,并变成红棕色气体.
在如图装置中,观察到图一装置铜电极上产生大量的无色气泡.而在图二装置中当开关K断开时,铬电极无现象,K闭合时,铬电极上产生大量无色气体,并变成红棕色气体.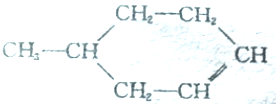 可以写成
可以写成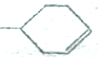 ,现有有机物A,可写为
,现有有机物A,可写为