题目内容
【题目】Ⅰ.如图1所示是中学化学中常用于混合物的分离和提纯的装置,请根据装置回答问题:
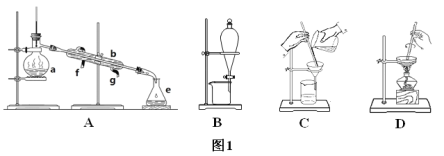
(1)从氯化钾溶液中得到氯化钾固体选择装置___(填代表装置图的字母,下同);除去自来水中的氯离子等杂质选择装置____。
(2)从碘水中分离出I2选择装置_____,该分离方法的名称为____。
(3)装置A中仪器a的名称是_____,进水的方向是____。
Ⅱ.海水中蕴藏着丰富的资源,在实验室中取少量海水,进行如图2流程的实验:

(1)粗盐中含Ca2+、Mg2+、SO42-等杂质,需要提纯后才能综合利用。粗盐提纯的步骤有: ①加入过量的Na2CO3溶液②加入过量的BaCl2溶液;③加入过量的NaOH溶液;④加入盐酸调节溶液至中性;⑤溶解;⑥过滤;⑦蒸发。正确的操作顺序是(填写序号字母)______。
a.⑤②③①④⑥⑦ b.⑤①②③⑥④⑦ c.⑤②①③④⑥⑦ d.⑤③②①⑥④⑦
(2)由海水到氯化钠晶体的实验过程中要用到的主要装置是(从图1中给定的四种装置中选择)____。
【答案】D A B 萃取、分液 蒸馏烧瓶 下口进水 d CD
【解析】
Ⅰ.(1)从氯化钾溶液中得到氯化钾固体采用蒸发溶剂的方法,所以选择装置D;除去自来水中的氯离子等杂质可以用蒸馏的方法,所以选择装置A。
(2)利用碘不易溶于水但易溶于有机溶剂的性质,从碘水中分离出I2可以选择合适的萃取剂进行萃取,然后分液,所以选择装置B,故答案为:B,萃取、分液。
(3)装置A中仪器a是蒸馏烧瓶,为了充分冷凝气体,冷凝管中水的流向和气体的流向应该相反,所以从冷凝管的下口进水。故答案为:蒸馏烧瓶,下口。
Ⅱ.(1)先把粗盐溶于水,用过量的NaOH溶液除去粗盐中含有的Mg2+,用过量的BaCl2溶液除去SO42-,用过量的Na2CO3溶液除去Ca2+和过量的Ba2+,然后过滤,再向滤液中加入盐酸至中性,除去过量的OH-和CO32-,最后蒸发掉水,得到纯净的NaCl。加Na2CO3溶液之前必须先加入BaCl2溶液,利用后加入的Na2CO3溶液除去先加入的过量的Ba2+,过量的CO32-可以利用过滤后加入的盐酸除去,NaOH溶液只要在过滤之前加入即可。所以选d。
(2)由海水到氯化钠晶体,需要先进行海水晒盐,得到的粗盐经提纯(除去粗盐中的泥沙和可溶性杂质离子Ca2+、Mg2+、SO42-等)得到食盐水,最后再蒸发得到纯净的食盐。除去粗盐中的泥沙和可溶性杂质离子Ca2+、Mg2+、SO42-等需要用到过滤的装置,从食盐水中得到食盐需要蒸发,所以选择装置CD。

 阅读快车系列答案
阅读快车系列答案