题目内容
15.在浓CaCl2溶液中通入NH3和CO2,可以制得纳米级碳酸钙.如图甲所示A-E为实验室常见的仪器装置(部分固定夹持装置略去),请根据要求回答问题.(1)实验室若用NH4Cl和熟石灰作试剂来制取、收集干燥的NH3,则需选用上述仪器装置中的BDE(填装置序号).若要制取、收集干燥的CO2,请选择装置并按气流方向连接各仪器接口acdh.
(2)若在A的分液漏斗内改加浓氨水,圆底烧瓶内加NaOH固体,也能制取氨气.请解释装置A中能产生氨气的原因氢氧化钠溶于水放出大量热,温度升高,使氨的溶解度减小而放出氢氧化钠电离出的OH-增大了氨水中OH-浓度,促使氨水电离平衡左移,导致氨气放出
(3)向浓CaCl2溶液中通入NH3和CO2气制纳米级碳酸钙时,应先通入的气体是NH3,若实验过程中有氨气逸出,应选图乙b装置回收(填代号).写出制纳米级碳酸钙的化学方程式CaCl2+CO2+2NH3+H2O=CaCO3+2NH4Cl.
(4)试设计简单的实验方案,判断所得碳酸钙样品颗粒是否为纳米级取少量样品和水混合形成分散系,用一束光照射,若出现一条光亮的通路,则是纳米级,否则不是.
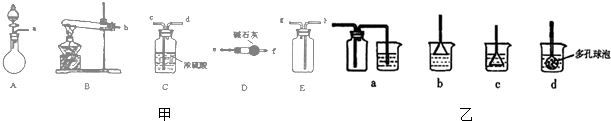
分析 (1)根据反应物的状态、反应条件选取反应装置,根据气体的溶解性、密度选择收集装置;若要制取、收集干燥的CO2,应选择ACE装置,按照制取、除杂、收集的顺序连接实验装置;
(2)NaOH溶于水放出大量的热,可促进氨气的挥发;
(3)根据二氧化碳和氨气的溶解性判断先通入的气体,由反应物和生成物写出反应方程式;
(4)碳酸钙样品颗粒如果为纳米级,纳米级的颗粒在胶体范围内,所以根据胶体的性质确定实验方案.
解答 解:(1)实验室制取氨气采用固体、固体加热型装置,所以应选B为反应装置;生成物中含有水,氨气属于碱性气体,所以应选择碱性物质吸收水蒸气,故选D;氨气极易溶于水,且氨气的密度小于空气的密度,所以应采用向下排空气法收集,故选E;若要制取、收集干燥的CO2,应选择ACE装置,按照制取、除杂、收集的顺序连接实验装置,因氨气密度比空气小,应用向上排空气法收集,则应为acdh,
故答案为:BDE;acdh;
(2)NaOH溶于水放出大量的热,可促进氨气的挥发,另外氨水溶液呈碱性,为弱电解质,加入氢氧化钠电离出的OH-增大了氨水中OH-浓度,促使氨水电离平衡左移,导致氨气放出,
故答案为:氢氧化钠溶于水放出大量热,温度升高,使氨的溶解度减小而放出;氢氧化钠电离出的OH-增大了氨水中OH-浓度,促使氨水电离平衡左移,导致氨气放出;
(3)氨气极易溶于水,二氧化碳不易溶于水,所以应先通入氨气;氨气极易溶于水,所以尾气处理应采用防止倒吸装置,用水吸收即可,应选择b,氨气溶于水生成氨水,溶液呈碱性,二氧化碳是酸性气体,能和碱反应生成碳酸铵,碳酸铵和氯化钙发生复分解反应生成碳酸钙和氯化铵,反应的方程式为CaCl2+CO2+2NH3+H2O=CaCO3↓+2NH4Cl,
故答案为:NH3;b;CaCl2+CO2+2NH3+H2O=CaCO3+2NH4Cl;
(4)碳酸钙样品颗粒如果为纳米级,纳米级的颗粒在胶体范围内,所以具有胶体的性质,运用胶体的丁达尔效应判断;取少量样品和水混合形成分散系,用一束光照射,若出现一条光亮的通路,则是纳米级,否则不是,
故答案为:取少量样品和水混合形成分散系,用一束光照射,若出现一条光亮的通路,则是纳米级,否则不是.
点评 本题考查了氨气的实验室制法,难度中等,注意根据反应物的状态、反应条件选取反应装置,根据气体的溶解性、密度选择收集装置.

 浙江之星课时优化作业系列答案
浙江之星课时优化作业系列答案 激活思维优加课堂系列答案
激活思维优加课堂系列答案| A. | 无色溶液中可能大量存在Al3+、NH4+、Cl?、S2? | |
| B. | 酸性溶液中可能大量存在Fe3+、K+、Cl?、SO42? | |
| C. | 弱碱性溶液中可能大量存在Na+、K+、Cl?、HCO3? | |
| D. | 酸性溶液中可能大量存在Na+、ClO?、SO42?、I? |
| A. | 试管外壁发热 | B. | 溶液最后变为蓝色 | ||
| C. | 溶液先变蓝最后褪色 | D. | 有气泡冒出 |
| A. | 碘水 | B. | 溴水 | C. | 碘化钾溶液 | D. | 氯水 |
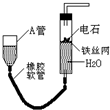 如图的实验装置可用于实验室中制取乙炔及成份检验.
如图的实验装置可用于实验室中制取乙炔及成份检验.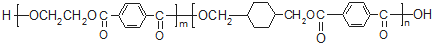
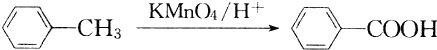
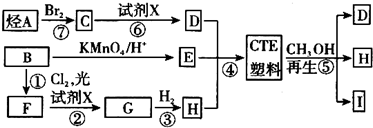
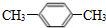 ,I的结构简式为
,I的结构简式为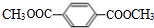 .
.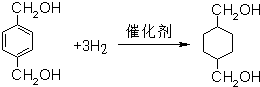 .
.