题目内容
【题目】锰氧化物(CuMn2O4)能在常温下催化氧化空气中的一氧化碳和甲醛(HCHO).
(1)锰元素位于第四周期第ⅦB族.基态Mn2+的核外电子排布式为 . NO3﹣的空间构型为 .
(2)HCHO中含有的σ键和π键数目之比为 .
(3)火山喷出的岩浆中含有多种硫化物,冷却时ZnS比HgS先析出,原因是
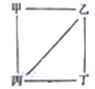
(4)Cu3N形成的晶体结构如图所示.则与同一个N3﹣相连的Cu+有个,Cu+的半径为a pm,N3﹣的半径为b pm,则Cu3N的密度为gcm﹣3 . (只列式,不用计算出结果)(阿伏加德罗常数用NA表示,1pm=10﹣10 cm) 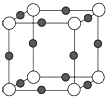
【答案】
(1)1s22s22p63s23p63d5;平面三角形
(2)3:1
(3)二者均为离子晶体,ZnS晶格能大于HgS,因此ZnS先析出
(4)6;![]()
【解析】解:(1.)Mn的原子序数为25,基态原子的电子排布式为,1s22s22p63s23p63d54s2 , 则Mn2+基态的电子排布式可表示为1s22s22p63s23p63d5(或[Ar]3d5),NO3﹣中N原子形成3个δ键,没有孤电子对,则应为平面三角形,所以答案是:1s22s22p63s23p63d5;平面三角形;
(2.)甲醛的结构式为 ![]() ,分子中含有2个C﹣H键、1个C=O键,单键为σ键,双键中具有1个σ键、1π键,故分子中σ键和π键数目比为3:1;所以答案是:3:1;
,分子中含有2个C﹣H键、1个C=O键,单键为σ键,双键中具有1个σ键、1π键,故分子中σ键和π键数目比为3:1;所以答案是:3:1;
(3.)二者均为离子晶体,ZnS晶格能大于HgS,因此ZnS先析出,所以答案是:二者均为离子晶体,ZnS晶格能大于HgS,因此ZnS先析出;
(4.)晶胞中黑色球数目为12× ![]() =3,白色球数目为8×
=3,白色球数目为8× ![]() =1,故黑色球为Cu+ , 白色球为N3﹣ , 由晶胞结构可知,棱上的Cu+与N3﹣相连,以N3﹣为中心,在X、Y、Z三个轴上,在每个轴上等距离的Cu+有2个,故同一个N3﹣相连的Cu+有6个,晶胞的体积=[(2a+2b)×10﹣10cm]3 , Cu3N的密度=
=1,故黑色球为Cu+ , 白色球为N3﹣ , 由晶胞结构可知,棱上的Cu+与N3﹣相连,以N3﹣为中心,在X、Y、Z三个轴上,在每个轴上等距离的Cu+有2个,故同一个N3﹣相连的Cu+有6个,晶胞的体积=[(2a+2b)×10﹣10cm]3 , Cu3N的密度= ![]() =
= ![]() g/cm3 , 所以答案是:6;
g/cm3 , 所以答案是:6; ![]() .
.

 名校课堂系列答案
名校课堂系列答案