题目内容
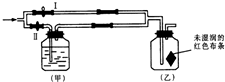
15. 如图是一种正在投入生产的大型蓄电系统的原理图.电池中的左右两侧为电极,中间为离子选择性膜,在电池放电和充电时该膜只允许钠离子通过.电池充、放电反应的化学方程式为:2Na2S2+NaBr3$?_{充电}^{放电}$Na2S4+3NaBr,下列关于此电池说法正确的是( )
如图是一种正在投入生产的大型蓄电系统的原理图.电池中的左右两侧为电极,中间为离子选择性膜,在电池放电和充电时该膜只允许钠离子通过.电池充、放电反应的化学方程式为:2Na2S2+NaBr3$?_{充电}^{放电}$Na2S4+3NaBr,下列关于此电池说法正确的是( )| A. | 充电过程中,当0.1 mol Na+通过离子交换膜时,导线通过0.1 mol电子 | |
| B. | 电池放电时,负极反应为:3NaBr一2e-═NaBr3+2Na+ | |
| C. | 充电过程中钠离子从右到左通过离子交换膜 | |
| D. | 放电过程中钠离子从左到右通过离子交换膜 |
分析 根据电池充、放电的化学反应方程式为2Na2S2+NaBr3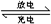 Na2S4+3NaBr可知,放电时为原电池反应:负极反应为2Na2S2-2e-=2Na++Na2S4,正极反应为NaBr3+2Na++2e-=3NaBr;充电时为电解池反应:阳极电极反应为:3NaBr-2e-=NaBr3+2Na+;阴极电极反应为:2Na++Na2S4+2e-=2Na2S2;根据原电池原理和电极原理分析判断.
Na2S4+3NaBr可知,放电时为原电池反应:负极反应为2Na2S2-2e-=2Na++Na2S4,正极反应为NaBr3+2Na++2e-=3NaBr;充电时为电解池反应:阳极电极反应为:3NaBr-2e-=NaBr3+2Na+;阴极电极反应为:2Na++Na2S4+2e-=2Na2S2;根据原电池原理和电极原理分析判断.
解答 解:A、有0.1molNa+通过离子交换膜,说明有0.1mol电子转移,故A正确;
B、放电时为原电池反应:负极反应为2Na2S2-2e-=2Na++Na2S4,故B错误;
C、依据图示方向,电极反应,充电过程中钠离子从左到右通过离子交换膜,故C错误;
D、依据原电池电极反应分析,放电过程中钠离子从右到左通过离子交换膜,故D错误;
故选A.
点评 本题考查了原电池和电解池的工作原理应用,电极反应电极判断是解题关键,题目难度中等.

练习册系列答案
 举一反三期末百分冲刺卷系列答案
举一反三期末百分冲刺卷系列答案
相关题目
10.设NA表示阿伏加德罗常数的值,下列叙述中正确的是( )
| A. | 常温常压下,48gO3含有的氧分子数为3NA | |
| B. | 标准状况下,1.8g的水中含有的氧原子数为0.1NA | |
| C. | 22.4 L O2中含有的氧气分子数约为6.02×1023 | |
| D. | 1mol O2氧气分子所占的体积数约为22.4 L |
7.下列说法正确的是( )
| A. | 电子层结构相同的离子,随核电荷数的增大其离子半径逐渐减小 | |
| B. | 分子间作用力越强,则分子结构越稳定 | |
| C. | 失电子能力弱的原子得电子能力一定强 | |
| D. | 通过离子键形成的晶体属于离子晶体,通过共价键形成的晶体属于分子晶体 |
4.物质的量浓度和体积均相同的下列溶液中,含阴离子种类最多的是( )
| A. | CaCl2 | B. | CH3COONa | C. | (NH4)2SO4 | D. | K2CO3 |
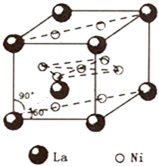 镍(Ni)是一种重要的金属,在材料科学等领域有广泛应用.
镍(Ni)是一种重要的金属,在材料科学等领域有广泛应用.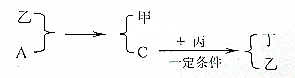
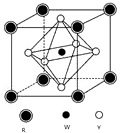 前四周期元素X、Y、Z、W、R的原子序数依次增大,已知:X原子的2p轨道为半充满状态;Y原子的L层有2个未成对电子;Z与Y位于同主族;W的+2价简单离子核外电子层排布与Ar原子相同;R原子的d轨道上有3个空轨道.请回答下列问题:
前四周期元素X、Y、Z、W、R的原子序数依次增大,已知:X原子的2p轨道为半充满状态;Y原子的L层有2个未成对电子;Z与Y位于同主族;W的+2价简单离子核外电子层排布与Ar原子相同;R原子的d轨道上有3个空轨道.请回答下列问题: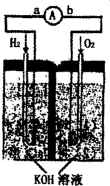 氢氧燃料电池是符合绿色化学理念的新型发电装置.如图为电池示意图,该电池电极表面镀一层细小的铂粉,吸附气体的能力强,性质稳定.请回答:
氢氧燃料电池是符合绿色化学理念的新型发电装置.如图为电池示意图,该电池电极表面镀一层细小的铂粉,吸附气体的能力强,性质稳定.请回答: