题目内容
【题目】二茂铁分子[Fe (C5H5)2]是一种金属有机配合物,是燃料油的添加剂,用以提高燃烧的效率和去烟,可作为导弹和卫星的涂料等。它的结构如图所示,下列说法正确的是( )
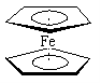
A.二茂铁中Fe2+与环戊二烯离子(C5H5-)之间为离子键
B.1mol环戊二烯(![]() )中含有σ键的数目为5NA
)中含有σ键的数目为5NA
C.二茂铁分子中存在π键
D.Fe2+的电子排布式为1s22s22p63s23p63d44s2
【答案】C
【解析】根据结构简式可知,分子中的化学键是配位键,A不正确。碳碳双键中含有1个σ键和1个π键,所以1mol环戊二烯(![]() )中含有σ键11mol,B不正确,C正确。根据构造原理可知,Fe2+的电子排布式为1s22s22p63s23p63d54s1。答案选C。
)中含有σ键11mol,B不正确,C正确。根据构造原理可知,Fe2+的电子排布式为1s22s22p63s23p63d54s1。答案选C。

练习册系列答案
 赢在课堂名师课时计划系列答案
赢在课堂名师课时计划系列答案 天天向上课时同步训练系列答案
天天向上课时同步训练系列答案 阳光课堂同步练习系列答案
阳光课堂同步练习系列答案
相关题目



