��Ŀ����
����Ŀ����֪ij�л���A�� ����C��H��O����Ԫ����ɣ���ȼ�շ���ʵ��ⶨ��̼������������64.86%���������������13.51%
����ͼ�Ǹ��л��������ͼ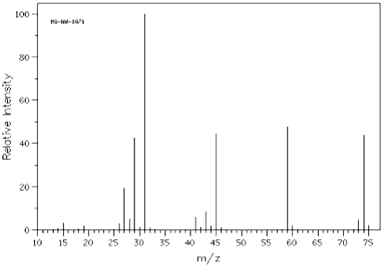
��A�ĺ������ͼ����C��H����O��H����C��O���������շ壮
��A�ĺ˴Ź��������������壮��ش�
��1��A��ʵ��ʽ�����ʽ��Ϊ �� ��Է�������Ϊ �� ����ʽΪ ��
��2����֪A�����ʽ�ܷ�ȷ��A�ķ���ʽ����ܡ����ܡ��� �� Ϊʲô ��
��3��A�Ľṹ��ʽΪ ��
���𰸡�
��1��C4H10O��74�� C4H10O
��2���ܣ���ΪA�����ʽΪC4H10O,��ԭ���Ѿ��ﵽ���ͣ�����A�����ʽ����A�ķ���ʽ
��3��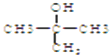
���������⣺��1��̼������������64.86%���������������13.51%����Ԫ������������21.63%�����������̼���⡢��ԭ�Ӹ���֮��= ![]() ��
�� ![]() ��
�� ![]() =4��10��1��������ʵ��ʽΪ��C4H10O��
=4��10��1��������ʵ��ʽΪ��C4H10O��
��������ͼ֪������Է���������74�������ʵ��ʽ֪�����ʽΪC4H10O��
���Դ��ǣ�C4H10O��74��C4H10O����2�����л�������ʽΪC4H10O��Hԭ���Ѿ�����Cԭ�ӵ��ļ۽ṹ�����ʽ��Ϊ����ʽ��
���Դ��ǣ��ܣ���ΪA�����ʽΪC4H10O����ԭ���Ѿ��ﵽ���ͣ�����A�����ʽ����A�ķ���ʽ����3���������ͼ����C��H����O��H����C��O���������շ��A�ĺ˴Ź��������������壬˵��A�к��ǻ��ͼ����ʸ��л���Ľṹ��ʽΪ��
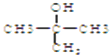 �����Դ��ǣ�
�����Դ��ǣ� 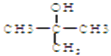 ��
��

����Ŀ������������գ�
��1��̼������Һ�и����Ӱ���Ũ�ȴӴ�С��˳������Ϊ�� ��
��2���±��Ǽ��ֳ�������ĵ���ƽ�ⳣ����25�棩
�� | H2CO3 | CH3COOH | HClO |
K | K1=4.4��10��7��K 2=4.7��10��11 | K=1.76��10��5 | K=2.95��10��8 |
���ݷ������������ݿ�֪��H2CO3��CH3COOH��HClO ����������Դ�ǿ������������25��ʱ����Ũ�ȵ�Na2CO3��NaAc ��NaClO������Һ��pH��С���������� ��
��3�������£���0.02molL��1 �� Ba��OH��2��Һ100mL��0.02molL��1��NaHSO4��Һ100mL��ϣ���������Һ����仯�����Ϻ����Һ�� pH Ϊ ��
��4��25��ʱ��Ksp[Mg��OH��2]=5.61��10��12 �� Ksp[MgF2]=7.42��10��11 �� ���¶��±���Mg��OH��2��Һ�뱥�� MgF2��Һ��ȣ����ѧʽ����Һ�е� c��Mg2+����