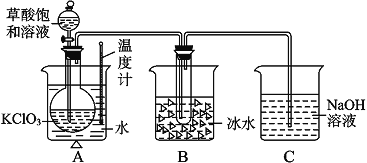
题目内容
【题目】在化学分析中,常需用KMnO4标准溶液,由于KMnO4晶体在室温下不太稳定,因而很难直接配置准确物质的量浓度的KMnO4溶液.实验室一般先称取一定质量的KMnO4晶体,配成大致浓度的KMnO4溶液,再用性质稳定、相对分子质量较大的基准物质草酸钠,对配制的KMnO4溶液进行标定,测出所配制的KMnO4溶液的准确浓度,反应原理为:5C2O42﹣+2MnO4﹣+16H+=10CO2↑+2Mn2++8H2O
以下是标定KMnO4溶液的实验步骤:
步骤一:先粗配浓度约为0.1molL﹣1的高锰酸钾溶液500mL.
步骤二:取0.2000molL﹣1的Na2C2O420.00mL放入锥形瓶中,并加稀硫酸酸化,用步骤一所配高锰酸钾溶液进行滴定.三次平行实验的数据记录在表中:
平行实验编号 | Na2C2O4溶液(mL) | 滴定管起始读数(mL) | 滴定管滴定终点读数(mL) |
1 | 20.00 | 0.00 | 23.18 |
2 | 20.00 | 1.02 | 21.00 |
3 | 20.00 | 1.18 | 21.20 |
试回答下列问题:
(1)步骤一中粗配溶液要用到的主要玻璃仪器除量筒外还需、 .
(2)高锰酸钾溶液应盛装于(填“酸式”或“碱式”)滴定管中:在使用滴定管前,应检查(填部位名称)是否漏水,在确保滴定管不漏水后方可使用;润洗滴定管内壁后的液体应从滴定管的(填“下部放入”或“上口倒入”)预置的烧杯中;步骤二中滴定终点的判断方法是: .
(3)下列滴定操作会导致测量结果偏高的是 .
A.滴定管滴定前有气泡,滴定后气泡消失
B.锥形瓶洗涤后没有干燥
C.滴定终点读数时俯视
D.滴定时锥形瓶中有液体溅出
(4)从实验所得数据计算,KMnO4溶液的浓度为molL﹣1 .
【答案】
(1)烧杯;玻璃棒
(2)酸式;活塞;下部放入;当滴入最后一滴KMnO4溶液时,待测液刚好出现紫色且半分钟内不褪色
(3)A
(4)0.08
【解析】解:(1)粗略配制高锰酸钾溶液,先计算所需高锰酸钾质量,利用量筒量取水500ml,用玻璃棒搅拌溶解得到溶液,所以需要的玻璃仪器为量筒、玻璃棒;所以答案是:烧杯;玻璃棒;(2)KMnO4溶液具有氧化性,应该用酸式滴定管盛装;在使用滴定管前,应检查活塞是否漏水;润洗滴定管内壁后的液体应从滴定管的下部放入预置的烧杯中,确保下端也被润洗;KMnO4溶液呈紫色,草酸反应完毕,当滴入最后一滴KMnO4溶液时,溶液由无色变为紫色,且半分钟内不褪色,即达滴定终点;所以答案是:酸;活塞;下部放入;当滴入最后一滴KMnO4溶液时,待测液刚好出现紫色且半分钟内不褪色;(3)A.滴定管滴定前有气泡,滴定后气泡消失,导致V(标准)偏大,根据c(待测)= ![]() 分析,可知c(待测)偏大,故A正确;B.锥形瓶洗涤后没有干燥,待测液的物质的量不变,标准液的体积不变,结果不变,故B错误;C.滴定终点读数时俯视,造成V(标准)偏小,根据c(待测)=
分析,可知c(待测)偏大,故A正确;B.锥形瓶洗涤后没有干燥,待测液的物质的量不变,标准液的体积不变,结果不变,故B错误;C.滴定终点读数时俯视,造成V(标准)偏小,根据c(待测)= ![]() 分析,可知c(待测)偏小,故C错误;D.滴定时锥形瓶中有液体溅出,待测液的物质的量偏小,造成V(标准)偏小,根据c(待测)=
分析,可知c(待测)偏小,故C错误;D.滴定时锥形瓶中有液体溅出,待测液的物质的量偏小,造成V(标准)偏小,根据c(待测)= ![]() 分析,可知c(待测)偏小,故D错误;故选A.(3)三次消耗高锰酸钾溶液的体积分别为:23.18mL、19.98mL、20.02mL,第一组误差较大,舍去,两次溶液的平均体积为20.00mL;
分析,可知c(待测)偏小,故D错误;故选A.(3)三次消耗高锰酸钾溶液的体积分别为:23.18mL、19.98mL、20.02mL,第一组误差较大,舍去,两次溶液的平均体积为20.00mL;
5C2O42﹣~2MnO4﹣5 2
0.2000molL﹣1×20.00mL C(KMnO4)×20.00mL
解得:C(KMnO4)=0.08molL﹣1
所以答案是:0.08;
【考点精析】关于本题考查的酸碱中和滴定,需要了解中和滴定实验时,用蒸馏水洗过的滴定管先用标准液润洗后再装标准液;先用待测液润洗后在移取液体;滴定管读数时先等一二分钟后再读数;观察锥形瓶中溶液颜色的改变时,先等半分钟颜色不变后即为滴定终点才能得出正确答案.

 阅读快车系列答案
阅读快车系列答案【题目】根据所学知识完成题目:
(1)某学生用0.20molL﹣1的标准NaOH溶液滴定未知浓度的盐酸,其操作为如下几步:
①用蒸馏水洗涤碱式滴定管,并立即注入NaOH溶液至“0”刻度线以上
②固定好滴定管并使滴定管尖嘴充满液体
③调节液面至“0”或“0”刻度线稍下,并记下读数
④移取20.00mL待测液注入洁净的锥形瓶中,并加入3滴酚酞溶液
⑤用标准液滴定至终点,记下滴定管液面读数.
请回答:
a.以上步骤有错误的是(填编号)
b.步骤⑤中,在记下滴定管液面读数时,滴定管尖嘴有气泡,将导致测定结果(填“偏大”、“偏小”或“无影响”)
c.下图是某次滴定时的滴定管中的液面,其读数为 mL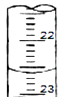
d.根据下列数据:请计算待测盐酸溶液的浓度: mol/L
滴定次数 | 待测体积(ml) | 标准烧碱体积(ml) | |
滴定前读数 | 滴定后读数 | ||
第一次 | 20.00 | 0.40 | 20.40 |
第二次 | 20.00 | 4.00 | 24.00 |
第三次 | 20.00 | 2.00 | 24.10 |
(2)按要求回答下列问题:
a.某温度时,水的离子积常数KW=10﹣13 , 将此温度下pH=11的Ba(OH)2溶液aL与pH=1的H2SO4溶液bL混合,设混合溶液体积为两者之和,所得固体体积忽略不计.若所得混合溶液为中性,则a:b=
b.已知在25℃的水溶液中,AgX、AgY、AgZ均难溶于水,且Ksp(AgX)=1.8×10﹣10 , Ksp(AgY)=1.0×10﹣12 , Ksp(AgZ)=8.7×10﹣17 . 则AgX、AgY、AgZ三者的溶解度(mol/L)S(AgX)、S(AgY)、S(AgZ)的大小顺序为:;若向AgY的饱和溶液中加入少量的AgX固体,则c(Y﹣)(填“增大”“减小”或“不变”).