题目内容
在密闭容器中发生如下反应:mA(g)+nB(g) pC(g),达到平衡后,保持温度不变,将气体体积缩小到原来的一半,当达到新平衡时,C的浓度为原来1.9倍,下列说法错误的是
pC(g),达到平衡后,保持温度不变,将气体体积缩小到原来的一半,当达到新平衡时,C的浓度为原来1.9倍,下列说法错误的是
| A.平衡向逆反应方向移动 | B.A的转化率降低 |
| C.m+n>p | D.C的体积分数减小 |
C
解析试题分析:平衡后将气体体积缩小到原来的一半,压强增大,如果平衡不移动,则达到平衡时C的浓度为原来的2倍,但此时C的浓度为原来的1.9倍,说明增大压强平衡向逆反应方向移动,A、由上述分析可知,增大压强平衡向逆反应方向移动,故A正确;B、增大压强平衡向逆反应方向移动,则反应物的转化率降低,故A的转化率降低,故B正确;C、增大压强平衡向逆反应方向移动,增大压强平衡向体积减小的方向移动,则有:m+n<p,故C不正确;D、平衡向逆反应移动,生成物的体积百分含量降低,即C的体积分数降低,故D正确,故选C。
考点:考查化学平衡移动的影响

 轻松暑假总复习系列答案
轻松暑假总复习系列答案T ℃时,将6 mol CO2和8 mol H2充入2 L密闭容器中,发生反应CO2(g)+3H2(g) CH3OH(g)+H2O(g),容器中H2的物质的量随时间变化如图中实线所示。图中虚线表示仅改变某一反应条件时,H2的物质的量随时间的变化。下列说法正确的是
CH3OH(g)+H2O(g),容器中H2的物质的量随时间变化如图中实线所示。图中虚线表示仅改变某一反应条件时,H2的物质的量随时间的变化。下列说法正确的是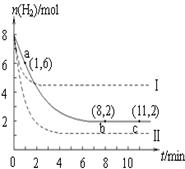
| A.反应开始至a点时v(H2)=1 mol·L-1·min-1 |
| B.若曲线Ⅰ对应的条件改变是升温,则该反应?H>0 |
| C.曲线Ⅱ对应的条件改变是降低压强 |
| D.T ℃时,该反应的化学平衡常数为0.125 |
为减小CO2对环境的影响,在倡导“低碳”的同时,还需加强对CO2创新利用的研究。已知:CO2(g)+3H2(g)  CH3OH(g)+H2O(g) △H=-49.0 kJ/mol。T1℃时,向体积为1L的恒容密闭容器中充入1molCO2和3molH2,测得CO2和CH3OH(g)的浓度随时间变化曲线如图所示,且平衡时体系压强为P1。下列叙述中不正确的是
CH3OH(g)+H2O(g) △H=-49.0 kJ/mol。T1℃时,向体积为1L的恒容密闭容器中充入1molCO2和3molH2,测得CO2和CH3OH(g)的浓度随时间变化曲线如图所示,且平衡时体系压强为P1。下列叙述中不正确的是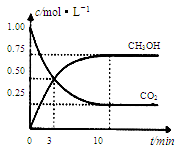
| A.0~3 min内,v(CO2)正 =v (CH3OH)正 |
| B.其他条件不变,若向平衡后的体系中充入1mol氦气,体系压强增大平衡将向正方向移动 |
| C.在T1℃时,若起始时向容器中充入2molCO2和6mol H2 , 测得平衡时容器内压强为P2, 则 P2<2P1 |
| D.T2℃时,上述反应平衡常数为4.2,则T2>T1 |
2007年度诺贝尔化学奖,授予致力于研究合成氨与催化剂表面积大小关系的德国科学家格哈德?埃特尔,表彰他在“固体表面化学过程”研究中作出的贡献。下列说法中正确的是
| A.工业生产中,合成氨采用压强越高,温度越低,越有利于提高经济效益。 |
| B.增大催化剂的表面积,能加快合成氨的正反应速率、降低逆反应速率 |
| C.采用催化剂时,反应的活化能降低,使反应易达过渡态,故明显加快 |
| D.增大催化剂的表面积,能增大氨气的产率 |
使反应4NH3(g)+3O2(g)=2N2(g)+6H2O(g)在2L的密闭容器中进行,半分钟后N2的物质的量增加了0.6mol。此反应的平均速率v(X)为
| A.v(NH3)=0.04mol·L-1·s-1 | B.v(O2)=0.015mol·L-1·s-1 |
| C.v(N2)=0.02mol·L-1·s-1 | D.v(H2O)=0.02mol·L-1·s-1 |
某反应A + B =" C" + D 在低温下能自发进行,在高温下不能自发进行,对该反应过程△H、△S的判断正确的是
| A.△H<0 △S<0 | B.△H>0 △S>0 |
| C.△H<0 △S>0 | D.△H>0 △S<0 |
煤气化的一种方法是在气化炉中给煤炭加氢,发生的主要反应为:C(s)+2H2(g) CH4(g)。在VL的容器中投入a mol碳(足量),同时通入2a molH2,控制条件使其发生上述反应,实验测得碳的平衡转化率随压力及温度的变化关系如图所示。下列说法正确的是
CH4(g)。在VL的容器中投入a mol碳(足量),同时通入2a molH2,控制条件使其发生上述反应,实验测得碳的平衡转化率随压力及温度的变化关系如图所示。下列说法正确的是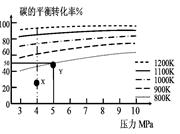
| A.上述正反应为吸热反应 |
| B.在4MPa、1200K时,图中X点υ(H2)正 >υ(H2)逆 |
C.在5MPa、800K时,该反应的平衡常数为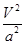 L2·mol-2 L2·mol-2 |
| D.工业上维持6MPa 1000K而不采用10MPa1000K,主要是因 |
对于可逆反应A(g)+2B(g) 2C(g)(正反应为吸热反应)达到平衡时,要使正反应速率降低,且使A的浓度增大,应采取的措施是( )
2C(g)(正反应为吸热反应)达到平衡时,要使正反应速率降低,且使A的浓度增大,应采取的措施是( )
| A.增大压强 | B.减少B的浓度 | C.减少A的浓度 | D.升高温度 |
 2C﹢D反应中,表示该反应速率最快的是( )
2C﹢D反应中,表示该反应速率最快的是( )