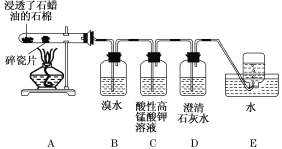
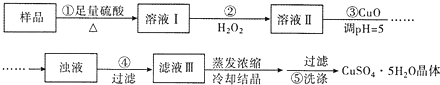
题目内容
【题目】I.下列物质:①16O和18O ②红磷和白磷 ③CH3CH3和CH3CH2CH2CH3 ④CH3CH2CH2CH3 和CH3CH (CH3) 2 ⑤O2和O3 ⑥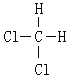 和
和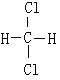
(1)属于同素异形体的是(填序号,下同) ,
(2)属于同系物的是 。
II.如图所示为CH4燃料电池的装置(A、B为多孔碳棒):
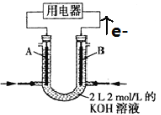
(1) (填A或B)处电极入口通甲烷,其电极反应式为 ;
(2)当消耗甲烷的体积为11.2 L(标准状况下)时,消耗KOH的质量为 g。
Ⅲ.铅蓄电池是最早使用的充电电池,由Pb、PbO2、稀硫酸构成。该电池工作时,若电路中转移2 mol电子,则负极材料质量的变化量为 g。
【答案】I.(1) ②⑤ (2) ③ II.(1)B CH4+10OH--8e-===CO32-+7H2O (2)56 Ⅲ.96
【解析】
试题分析:I.(1)红磷和白磷是磷元素形成的不同单质,互为同素异形体;O2和O3是氧元素形成的不同单质,二者互为同素异形体。
(2)结构相似,分子组成相差若干个CH2原子团的有机物互为同系物,CH3CH3和CH3CH2CH2CH3均属于烷烃,结构相似,二者互为同系物。
II.(1)根据电子的流向可知B电极是负极,则B处电极入口通甲烷。由于电解质溶液显碱性,则其电极反应式为CH4+10OH--8e-===CO32-+7H2O;
(2)当消耗甲烷的体积为11.2 L(标准状况下)时,甲烷的物质的量是0.5mol,根据总的反应式CH4+2KOH+2O2=K2CO3+3H2O可知消耗KOH是1mol,其质量为56g。
Ⅲ.铅蓄电池的负极是铅失去电子,转化为硫酸铅,电极反应式为Pb-2e-+SO42-=PbSO4。该电池工作时,若电路中转移2 mol电子,则负极消耗1mol铅,产生1mol硫酸铅,因此负极材料质量的变化量为参加反应的硫酸根的质量,质量为96g。