题目内容
【题目】1909年化学家哈伯在实验室首次合成了氨。2007年化学家格哈德·埃特尔在哈伯研究所证实了氢气与氮气在固体表面合成氨的反应过程,示意如下图:
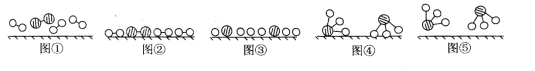
(1)图⑤表示生成的NH3离开催化剂表面,图②和图③的含义分别是______,_______。
(2)已知:4NH3(g)+3O2(g)=2N2(g)+6H2O(g);ΔH=-1266.8kJ/mol,N2(g)+O2(g)=2NO(g)ΔH=+180.5kJ/mol,氨催化氧化的热化学方程式为_________________________。
(3)500℃下,在A、B两个容器中均发生合成氨的反应。隔板Ⅰ固定不动,活塞Ⅱ可自由移动。
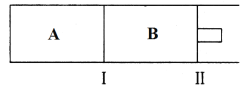
①当合成氨在容器B中达平衡时,测得其中含有1.0molN2,0.4molH2,0.4molNH3,此时容积为2.0L。则此条件下的平衡常数为________________;保持温度和压强不变,向此容器中通入0.36molN2,平衡将______________(填“正向”、“逆向”或“不”)移动。
②向A、B两容器中均通入xmolN2和ymolH2,初始A、B容积相同,并保持温度不变。若要平衡时保持N2在A、B两容器中的体积分数相同,则x与y之间必须满足的关系式为_____________。
(4)以CO和O2为电极燃料,以熔融K2CO3为电解质组成燃料电池,请写出该电池的负极反应方程式_____________________________________________。
【答案】N2和H2被吸附在催化剂表面 在催化剂表明N2和H2中化学键断裂 4NH3(g)+5O2(g)=4NO(g)+6H2O(g) H= —905.8KJ/mol 10 逆向 x=y CO-2e+CO32-=2CO2
【解析】
(1)图②表示N2、H2被吸附在催化剂表面,而图③表示在催化剂表面,N2、H2中化学键断裂;
(2)利用盖斯定律,把第二个热化学方程式两边扩大2倍,然后两个方程式相加就可以得到氨催化氧化的热化学方程式;
(3)①根据平衡常数的概念计算,根据计算的浓度商和平衡常数比较分析判断反应进行的方向;
②利用化学平衡三段式计算A的体积分数相等列式计算;
(4)根据CO在负极发生氧化反应写出电极方程式。
(1)分析题中图可以知道,图②表示N2、H2被吸附在催化剂表面,而图③表示在催化剂表面,N2、H2中化学键断裂,
故答案为:N2和H2被吸附在催化剂表面;在催化剂表面,N2和H2中化学键断裂。
(2)已知:4NH3(g)+3O2(g)=2N2(g)+6H2O(g)△H=-1266.8kJ/mol ①
N2(g)+O2(g)=2NO(g)△H=+180.5kJ/mol ②,由①+②×2得:4NH3(g)+5O2(g)=4NO(g)+6H2O(g)△H=-905.8kJ/mol,故答案为:4NH3(g)+5O2(g)=4NO(g)+6H2O(g)△H=-905.8kJ/mol。
(3)①若在某件下,反应A(g)+3B(g)2C(g)在容器N中达到平衡,测得容器中含有A1.0mol,B0.4mol,C0.4mol,此时容积为2.0L.则此条件下的平衡常数K=(0.4mol÷2L)2/(1mol÷2L)×(0.4mol÷2L)3=10;保持温度和压强不变,向此容器内通入0.36molA,平衡将Q=(1.36mol÷2L)2/(1mol÷2L)×(0.4mol÷2L)3=115.6>10,反应逆向进行;
故答案为:10;逆向。
②向M、N中,各通入xmolA和ymolB,初始M、N容积相同,并保持温度不变。设M容器中消耗A物质的量amol,N容器中消耗A物质的量为bmol,
M容器中,
A(g)+3B(g)2C(g)
起始量(mol) x y 0
变化量(mol) a 3a 2a
平衡量(mol) x-a y-3a 2a
N容器中,
A(g)+3B(g)2C(g),
起始量(mol) x y 0
变化量(mol) b 3b 2b
平衡量(mol)x-b y-3b 2b
若要平衡时保持A气体在M、N两容器中的体积分数相等,(x-a)/(x+y-2a)=(x-b)/(x+y-2b),x:y=(b-a):(b-a),则x:y=1:1,则起始通入容器中的A的物质的量x mol与B的物质的量y mol之间必须满足的关系式为x=y=1;故答案为:x=y。
(4)该燃料电池燃料为CO,电解质为熔融的K2CO3,总反应为2CO+O2=2CO2,CO在负极失电子发生氧化反应,负极反应方程式为:CO-2e+CO32-=2CO2,故答案为:CO-2e+CO32-=2CO2。