题目内容
【题目】依据氧化还原反应:2Ag+(aq)+Cu(s)=Cu2+(aq)+2Ag(s)设计的原电池如图。请回答下列问题:
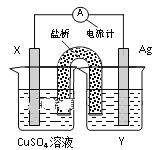
(1)电极X的材料名称是___;电解质溶液Y溶质的化学式是___;
(2)银电极为电池的___极,发生的电极反应为___;
(3)外电路中的电子是从___电极流向___电极。(填电极材料名称)。
(4)当有1.6g铜溶解时,银棒增重___g。
【答案】铜 AgNO3 正极 Ag++e-=Ag 铜 银 5.4
【解析】
(1)根据电池反应式知,Cu失电子发生氧化反应,作负极,Ag作正极,电解质溶液为含有银离子的可溶性银盐溶液;
(2)银电极上是溶液中的Ag+得到电子发生还原反应;
(3)外电路中的电子是从负极经导线流向正极;
(4)先计算Cu的物质的量,根据反应方程式计算出正极产生Ag的质量,即正极增加的质量。
(1)根据电池反应式知,Cu失电子发生氧化反应,Cu作负极,则Ag作正极,所以X为Cu,电解质溶液为AgNO3溶液,故答案为:铜;AgNO3;
(2)银电极为正极,正极上Ag+得到电子发生还原反应,正极的电极反应式为:Ag++e-=Ag,故答案为:正;Ag++e-=Ag;
(3)外电路中的电子是从负极Cu经导线流向正极Ag,故答案为:铜;银;
(4)反应消耗1.6 g铜的物质的量为n(Cu) =![]() =0.025 mol,根据反应方程式2Ag+(aq)+Cu(s)=Cu2+(aq)+2Ag(s)可知:每反应消耗1 mol Cu,正极上产生2 mol Ag,则0.025 mol Cu反应,在正极上产生0.05 mol Ag,该Ag的质量为m(Ag)=0.05 mol×108 g/mol=5.4 g,即正极银棒增重5.4 g,故答案为:5.4。
=0.025 mol,根据反应方程式2Ag+(aq)+Cu(s)=Cu2+(aq)+2Ag(s)可知:每反应消耗1 mol Cu,正极上产生2 mol Ag,则0.025 mol Cu反应,在正极上产生0.05 mol Ag,该Ag的质量为m(Ag)=0.05 mol×108 g/mol=5.4 g,即正极银棒增重5.4 g,故答案为:5.4。

练习册系列答案
相关题目