题目内容
用铂作电极电解1L含有0.4molCuSO4和0.2molNaCl的水溶液,一段时间后在一个电极上得到了19.2 g Cu,在另一极上析出的气体在标况下的体积是
| A.4.48 L | B.5.6 L | C.6.72 L | D.13.44 L |
A
试题分析:将含有0.2mol NaCl和0.4mol CuSO4的水溶液1L,用惰性电极电解,溶液中的阳离子有Cu2+、H+、Na+;移向阴极,发生的电极反应为:Cu2++2e-=Cu。
阴离子Cl-、OH-、NO3-;移向阳极;电极反应为:2Cl--2e-=Cl2↑,0.3molCu生成转移电子为0.6mol;溶液中氯离子物质的量为0.2mol,全部反应失去电子物质的量为0.2mol,生成氯气为0.1mol,还有0.4mol电子是氢氧根离子失去发生电极反应为:4OH--4e-=2H2O+O2↑生成氧气为0.1mol,所以共生成气体标准状况下生成气体体积为(0.1mol+0.1mol)×22.4L/mol=4.48L;
故选B。
点评:本题考查了电解原理的应用,混合电解电极产物的判断与计算,主要是离子放电顺序和电子守恒的应用书写电极反应和进行有关计算。

练习册系列答案
相关题目
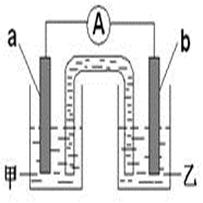
 2H2O ,设计出以稀硫酸为电解质溶液的燃料电池,其电极反应式为:负极 ,正极 。
2H2O ,设计出以稀硫酸为电解质溶液的燃料电池,其电极反应式为:负极 ,正极 。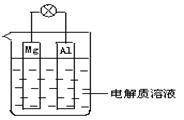

 3Zn(OH)2 + 2Fe(OH)3 + 4KOH,下列叙述不正确的是
3Zn(OH)2 + 2Fe(OH)3 + 4KOH,下列叙述不正确的是