题目内容
【题目】0.2mol 某烃 A 在氧气中完全燃烧后,生成CO2和H2O各1.2mol 。试回答:
(1)烃A的分子式为______________。
(2)若取一定量的该烃 A完全燃烧后,生成CO2和H2O各3mol ,则有______ g 烃 A参加了反应,燃烧时消耗标准状况下的氧气______ L 。
(3)若烃 A 不能使溴水褪色,但在一定条件下能与氯气发生取代反应,其一氯取代物只有一种,则烃 A 的结构简式为______。
(4)若烃 A 能使溴水褪色,在催化剂作用下,与H2加成,其加成产物经测定分子中含有 4个甲基,烃A可能有的结构简式为(写一种即可)______________。
(5)比烃 A 少一个碳原子且能使溴水褪色的 A 的同系物有______种同分异构体(包括顺反异构)。
【答案】C6H12 42 100.8 ![]() (CH3)3CCH=CH2或(CH3)2CHC(CH3)=CH2或(CH3)2C=C(CH3)2 5
(CH3)3CCH=CH2或(CH3)2CHC(CH3)=CH2或(CH3)2C=C(CH3)2 5
【解析】
(1)根据原子守恒确定烃A分子中C、H原子数目,可知烃A分子式为C6H12;
(2)根据C原子守恒计算参加反应的烃A的物质的量,再根据m=n·M计算参加反应烃A的质量,根据物质反应前后质量守恒计算O2的物质的量,结合V=n·Vm计算消耗的氧气的体积;
(3)烃A不能使溴水褪色,不含不饱和键,在一定条件下能与氯气发生取代反应,其一氯取代物只有一种,A为环己烷;
(4)烃A能使溴水褪色,含有1个C=C双键,在催化剂作用下,与H2加成,其加成产物经测定分子中含有4个甲基,故加成产物的结构简式为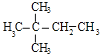 或
或![]() ,相邻C原子上各去掉1个H原子,还原碳碳双键;
,相邻C原子上各去掉1个H原子,还原碳碳双键;
(5)比烃A少一个碳原子且能使溴水褪色的A的同系物,分子式为C5H10,含有1个C=C双键。
(1)0.2mol某烃A在氧气中完全燃烧后,生成CO2和H2O各1.2mol,根据原子守恒确定A分子中C原子数目为C:1.2mol÷0.2mol=6;含有的H原子数目为H:(1.2mol×2)÷0.2mol=12,所以该烃A分子式为C6H12;
(2)根据C原子守恒,可知参加反应的烃A的物质的量为n(C6H12)=3mol÷6=0.5mol,则参加反应烃A的质量为m(C6H12)=0.5mol×84g/mol=42g,烃C6H12燃烧的化学方程式为C6H12+9O2![]() 6CO2+6H2O,根据方程式可知1molC6H12完全燃烧消耗9molO2,则0.5molC6H12燃烧消耗4.5molO2,其在标准状况下的体积V(O2)=4.5mol×22.4L/mol=100.8L;
6CO2+6H2O,根据方程式可知1molC6H12完全燃烧消耗9molO2,则0.5molC6H12燃烧消耗4.5molO2,其在标准状况下的体积V(O2)=4.5mol×22.4L/mol=100.8L;
(3)烃A分子式为C6H12,烃A不能使溴水褪色,不含不饱和键,在一定条件下能与氯气发生取代反应,其一氯取代物只有一种,A为环己烷,结构简式为![]() ;
;
(4)烃A能使溴水褪色,物质分子中含有1个碳碳双键,在催化剂作用下,与H2加成,其加成产物经测定分子中含有4个甲基,故加成产物的结构简式为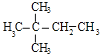 或
或![]() ,若加成产物为
,若加成产物为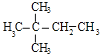 ,对应的A的结构为(CH3)3CCH=CH2;若加成产物为
,对应的A的结构为(CH3)3CCH=CH2;若加成产物为![]() ,则A可能为(CH3)2CHC(CH3)=CH2或(CH3)2C=C(CH3)2;
,则A可能为(CH3)2CHC(CH3)=CH2或(CH3)2C=C(CH3)2;
(5)比烃A少一个碳原子且能使溴水褪色的A的同系物,分子式为C5H10,含有1个碳碳双键,符合条件的同分异构体为:CH3CH2CH2CH=CH2、CH3CH2CH=CHCH3、CH2=C(CH3)CH2CH3、(CH3)2C=CHCH3、(CH3)2CHCH=CH2,共有5种不同结构。

【题目】T K时,向2.0 L恒容密闭容器中充入0.10 mol COCl2,发生反应COCl2(g)![]() Cl2(g)+CO(g),经过一段时间后反应达到平衡。反应过程中测得的部分数据见下表:
Cl2(g)+CO(g),经过一段时间后反应达到平衡。反应过程中测得的部分数据见下表:
t/s | 0 | 2 | 4 | 6 | 8 |
n(Cl2)/mol | 0 | 0.030 | 0.039 | 0.040 | 0.040 |
下列说法正确的是( )
A. 保持其他条件不变,升高温度,平衡时c(Cl2)=0.038 mol·L-1,则反应的ΔH<0
B. 反应在前2 s的平均速率v(CO)=0.015 mol·L-1·s-1
C. 保持其他条件不变,起始时向容器中充入0.12 mol COCl2、0.06 mol Cl2和0.06 mol CO,反应达到平衡前的速率:v正<v逆
D. 保持其他条件不变,起始时向容器中充入0.10 mol Cl2和0.08 mol CO,达到平衡时,Cl2的转化率大于60%