题目内容
8.恒温下,将a mol N2与b mol H2的混合气体通入一个固定容积的密闭容器中,发生如下反应:N2(g)+3H2(g)?2NH3(g)(1)写出该反应的平衡常数的表达式.$\frac{{c}^{2}(N{H}_{3})}{c({N}_{2})×{c}^{3}({H}_{2})}$
(2)若反应进行到某时刻t时,nt(N2)=13mol,nt(NH3)=6mol,则a=16.
(3)反应达平衡时,混合气体的体积为716.8L(标况下),其中NH3的含量(体积分数)为25%.计算平衡时n(NH3)=8mol.
(4)原混合气体与平衡混合气体的总物质的量之比5:4
(5)平衡混合气体中,n(N2):n(H2):n(NH3)=3:3:2.
分析 (1)化学平衡常数是指:一定温度下,可逆反应到达平衡时,生成物的浓度系数次幂之积与反应物的浓度系数次幂之积的比,固体、纯液体不需要在化学平衡常数中写出;
(2)恒温下,将a mol N2与b mol H2的混合气体通入一个固定容积的密闭容器中,若反应进行到某时刻t时,nt(N2)=13mol,nt(NH3)=6mol,则:
N2(g)+3H2(g)??2ΝΗ3(g)
起始量(mol):a b 0
变化量(mol):3 9 6
t时刻(mol):13 b-9 6
氮气起始物质的量=t时氮气物质的量+消耗氮气物质的量;
(3)根据n=$\frac{V}{{V}_{m}}$计算平衡时混合气体总物质的量,氨气物质的量=混合气体总物质的量×氨气体积分数;
(4)由(2)可知平衡时氨气物质的量,表示出平衡时各物质的物质的量,根据平衡时混合气体总物质的量计算b,恒温恒容下,压强之比等于物质的量之比;
(5)结合(4)中计算结果进行解答.
解答 解:(1)N2(g)+3H2(g)?2NH3(g)的平衡常数表达式K=$\frac{{c}^{2}(N{H}_{3})}{c({N}_{2})×{c}^{3}({H}_{2})}$,故答案为:$\frac{{c}^{2}(N{H}_{3})}{c({N}_{2})×{c}^{3}({H}_{2})}$;
(2)恒温下,将a mol N2与b mol H2的混合气体通入一个固定容积的密闭容器中,若反应进行到某时刻t时,nt(N2)=13mol,nt(NH3)=6mol,则:
N2(g)+3H2(g)??2ΝΗ3(g)
起始量(mol):a b 0
变化量(mol):3 9 6
t时刻(mol):13 b-9 6
则a=3+13=16,
故答案为:16;
(3)平衡时混合气体物质的量为$\frac{716.8L}{22.4L/mol}$=32mol,氨气物质的量为32mol×25%=8mol,
故答案为:8mol;
(4)氨气物质的量为32mol×25%=8mol,则:
N2(g)+3H2(g)??2ΝΗ3(g)
起始量(mol):16 b 0
变化量(mol):4 12 8
平衡时(mol):12 b-12 8
则12+b-12+8=32,解得b=24,
恒温恒容下,压强之比等于物质的量之比,则P(始):P(平)=(16+24)mol:32mol=5:4,
故答案为:5:4;
(5)由(4)计算可知,平衡混合气体中n(N2):n(H2):n(NH3)=12mol:12mol:8mol=3:3:2,
故答案为:3:3:2.
点评 本题考查化学平衡的计算、平衡常数,题目难度不大,注意三段式解题法在化学平衡计算中应用.

 培优三好生系列答案
培优三好生系列答案 优化作业上海科技文献出版社系列答案
优化作业上海科技文献出版社系列答案| A. | 30% | B. | 40% | C. | 53.3% | D. | 36.4% |
| A. | 用KIO3氧化酸性溶液中的KI:5I-+IO${\;}_{3}^{+}$+3H2O═3I2+6OH- | |
| B. | 向NH4HSO3溶液中加过量的NaOH溶液并加热:NH${\;}_{4}^{+}$+OH-$\frac{\underline{\;\;△\;\;}}{\;}$NH3↑+H2O | |
| C. | 将过量SO2通入冷氨水中:SO2+NH3•H2O═HSO${\;}_{3}^{-}$+NH${\;}_{4}^{+}$ | |
| D. | Ba(OH)2溶液中逐滴加入一定物质的量浓度的NaHSO4溶液,当溶液中的OH-恰好反应一半时:Ba2++2OH-+2H++SO${\;}_{4}^{2-}$═BaSO4↓+2H2O |
| A. | 加入氯化钡溶液有白色沉淀产生,再加盐酸,沉淀不消失,一定有SO42- | |
| B. | 加入稀盐酸产生无色气体,将气体通入澄清石灰水中,溶液变浑浊,一定有CO32- | |
| C. | 加入氢氧化钠溶液并加热,产生的气体能使湿润红色石蕊试纸变蓝,一定有NH4+ | |
| D. | 加入碳酸钠溶液产生白色沉淀,再加盐酸白色沉淀消失,一定有Ba2+ |
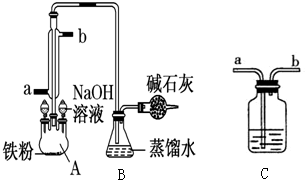 某化学课外小组用如图所示的装置制取溴苯.先向分液漏斗中加入苯和液溴,再将两液体慢慢滴入反应器A(A下端活塞关闭)中.
某化学课外小组用如图所示的装置制取溴苯.先向分液漏斗中加入苯和液溴,再将两液体慢慢滴入反应器A(A下端活塞关闭)中.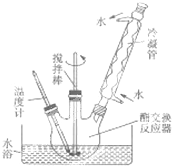 生物柴油是高级脂肪酸甲酯,可由油脂与甲醇通过取代反应(酯交换,生成新酯和新醇)得到,用菜籽油制备生物柴油的步骤如下:
生物柴油是高级脂肪酸甲酯,可由油脂与甲醇通过取代反应(酯交换,生成新酯和新醇)得到,用菜籽油制备生物柴油的步骤如下: