题目内容
3.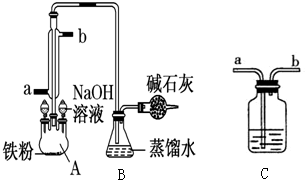 某化学课外小组用如图所示的装置制取溴苯.先向分液漏斗中加入苯和液溴,再将两液体慢慢滴入反应器A(A下端活塞关闭)中.
某化学课外小组用如图所示的装置制取溴苯.先向分液漏斗中加入苯和液溴,再将两液体慢慢滴入反应器A(A下端活塞关闭)中.(1)实验开始前应对装置进行气密性检查,其操作是:关闭左右侧分液漏斗玻璃活塞,导气管插入锥形瓶水中,微热三颈瓶观察导气管口是否有气泡冒出,停止加热导气管中若上升一段水柱,说明气密性完好
(2)写出A中反应的化学方程式:C6H6+Br2→C6H5Br+HBr.
(3)冷凝水的进水口是a(填a或b)
(4)反应结束后,往A中加入NaOH溶液,充分振荡,目的是提纯溴苯写出有关反应的化学方程式:Br2+2NaOH=NaBr+NaBrO+H2O.
(5)有同学认为该实验存在一定的缺点,应在A与B之间连接一个C装置,则C中应装有CCl4,其目的是除去溴化氢气体中的溴蒸气.
分析 根据实验装置可知,将溴和苯的混合物滴入到铁丝上,在铁作催化剂的条件下苯和溴发生取代反应生成溴苯和溴化氢,溴和苯都是易挥发的物质,所以C装置中用四氯化碳吸收溴化氢气体中的苯和溴,生成的溴化氢用水吸收,注意要防止倒吸,所以导管口中液面上方,A中反应后的溶液放到B中,用氢氧化钠溶液除去溴苯中的溴,
(1)密闭装置,最后导气管插入水中,关闭三颈瓶中气体压强,观察导气管处的气泡和是否上升一段水柱,判断气密性,
(2)铁与溴反应生成溴化铁,溴和苯在溴化铁催化作用下反应生成溴苯和溴化氢;
(3)冷凝器中水流应遵循逆流方向;
(4)生成的溴苯中含有苯、溴等杂质,在A中与氢氧化钠充分作用,可除去溴,用于提纯溴苯;
(5)要检验溴化氢的存在应先除去溴,挥发的溴易溶于四氯化碳.
解答 解:(1)实验开始前应对装置进行气密性检查,其操作是:关闭左右侧分液漏斗玻璃活塞,导气管插入锥形瓶水中,微热三颈瓶观察导气管口是否有气泡冒出,停止加热导气管中若上升一段水柱,说明气密性完好,
故答案为:关闭左右侧分液漏斗玻璃活塞,导气管插入锥形瓶水中,微热三颈瓶观察导气管口是否有气泡冒出,停止加热导气管中若上升一段水柱,说明气密性完好;
(2)铁与溴反应生成溴化铁,溴和苯在溴化铁催化作用下反应生成溴苯和溴化氢,A中反应的化学方程式:溴和苯在溴化铁催化作用下反应生成溴苯和溴化氢,反应的方程式为C6H6+Br2→C6H5Br+HBr,
故答案为:C6H6+Br2→C6H5Br+HBr;
(3)冷凝器中水流应遵循逆流方向,冷凝水的进水口应为a处,
故答案为:a;
(4)溴苯中含有溴,溴可与氢氧化钠反应而被除去,反应的化学方程式为:Br2+2NaOH=NaBr+NaBrO+H2O,
故答案为:提纯溴苯,Br2+2NaOH=NaBr+NaBrO+H2O;
(5)根据相似相溶原理,溴极易溶于四氯化碳,而溴化氢则不溶,所以C中盛放CCl4的作用是除去溴化氢气体中的溴蒸气,
故答案为:CCl4,除去溴化氢气体中的溴蒸气.
点评 本题考查苯的取代反应方程式及实验现象以及产物HBr的检验,题目难度中等,注意掌握苯的取代反应原理,明确反应的产物及HBr的化学性质进行解题.

 小学生10分钟口算测试100分系列答案
小学生10分钟口算测试100分系列答案| A. | 容器内的压强不随时间而变化 | B. | 混合气体的密度不再随时间而变化 | ||
| C. | P和R的生成速率相等 | D. | 容器内P、Q、R、S共存 |
①盐酸;②CuSO4溶液;③氢氧化钠溶液;④AgNO3溶液.
| A. | ①② | B. | ②③ | C. | ①③ | D. | ②④ |
 实验室制备1,2-二溴乙烷的反应原理如下:
实验室制备1,2-二溴乙烷的反应原理如下:CH3CH2OH$→_{170℃}^{H_{2}SO_{4}(浓)}$CH2=CH2,CH2=CH2+Br2→BrCH2CH2Br
可能存在的主要副反应有:乙醇在浓硫酸的存在下在140℃脱水生成乙醚.用少量溴和足量的乙醇制备1,2-二溴乙烷的装置如图所示:
有关数据列表如下:
| 乙醇 | 1,2-二溴乙烷 | 乙醚 | |
| 状态 | 无色液体 | 无色液体 | 无色液体 |
| 密度g/cm3 | 0.79 | 2.2 | 0.71 |
| 沸点/℃ | 78.5 | 132 | 34.6 |
| 熔点/℃ | -130 | 9 | -116 |
(1)在此制备实验中,要尽可能迅速地把反应温度提高到170℃左右,其最主要目的是d
a.引发反应 b.加快反应速度c.防止乙醇挥发 d.减少副产物乙醚生成
(2)在装置C中应加入c,(填序号)其目的是吸收反应中可能生成的酸性气体
a.水 b.浓硫酸c.氢氧化钠溶液 d.饱和碳酸氢钠溶液
(3)判断该制备反应已经结束的最简单方法是溴的颜色完全褪去
(4)将1,2-二溴乙烷粗产品置于分液漏斗中加水,振荡后静置,产物应在下层(填“上”、“下”)
(5)若产物中有少量未反应的Br2,最好用b洗涤除去(填序号)
a.水b.氢氧化钠溶液c.碘化钠溶液d.乙醇
(6)若产物中有少量副产物乙醚,可用蒸馏的方法除去
(7)反应过程中应用冷水冷却装置D,其主要目的是乙烯与溴反应时放热,冷却可避免溴的大量挥发但又不能过度冷却(如用冰水),其原因是1,2-二溴乙烷的凝固点较低(9℃),过度冷却会使其凝固而使气路堵塞.
| A. | 标准状况下,22.4 L H2和CO混合气体中的原子数 | |
| B. | 1.6 gCH4中含有的电子数 | |
| C. | 24 g金属镁与足量的盐酸反应转移的电子数 | |
| D. | 1 mol•L-1的稀硫酸100 mL中含有H+的数目 |
| A. | 电解精炼铜时,若阳极质量减少64g,则转移到阴极的电子不一定等于2NA | |
| B. | 1molNa2O2晶体中共含有4NA个离子 | |
| C. | 1.0L1.0mol/L的NaAlO2水溶液中含有的氧原子数为2NA | |
| D. | 常温下pH=1的H2SO4溶液中,H+的浓度为0.2mol/L |