题目内容
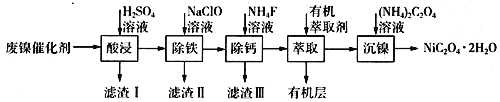
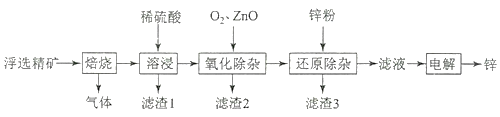
【题目】我国是世界上最早制得和使用金属锌的国家,一种以闪锌矿(ZnS,含有SiO2和少量FeS、CdS、PbS杂质)为原料制备金属锌的流程如图所示,下列有关说法不正确的是( )
A.滤渣1的成分是SiO2 , 滤渣2的成分是Fe(OH)3
B.焙烧过程中主要反应的化学方程式为2ZnS+3O2![]() 2ZnO+2SO2
2ZnO+2SO2
C.溶液中的Cd2+可用锌粉除去,反应的离子方程式为Zn+Cd2+=Zn2++Cd
D.若不通入氧气,其后果是无法除去杂质Fe2+
【答案】A
【解析】
闪锌矿主要含有ZnS,还含有SiO2和少量FeS、CdS、PbS杂质,焙烧过程中发生的反应有2ZnS+3O2![]() 2ZnO+2SO2、4FeS+7O2
2ZnO+2SO2、4FeS+7O2![]() 2Fe2O3+4SO2、2PbS+3O2
2Fe2O3+4SO2、2PbS+3O2![]() 2PbO+2SO2、2CdS+3O2
2PbO+2SO2、2CdS+3O2![]() 2CdO+2SO2,所以焙烧过程中生成的气体是SO2;然后加入稀硫酸酸浸,FeS(未焙烧)、ZnO、Fe2O3、PbO、CdO和稀硫酸反应生成Fe2+、Zn2+、Fe3+、PbSO4、Cd2+,所以滤渣1为未反应的SiO2和生成的PbSO4;氧化除杂时,通入氧气,使Fe2+转化为Fe3+,加入ZnO调节溶液的pH值,将Fe3+转化为Fe(OH)3而除去Fe3+,滤渣2为生成的Fe(OH)3;然后向溶液中加入Zn,Zn和Cd2+发生氧化还原生成Cd,然后过滤得到滤液,滤渣3为Cd;将滤液电解得到Zn。
2CdO+2SO2,所以焙烧过程中生成的气体是SO2;然后加入稀硫酸酸浸,FeS(未焙烧)、ZnO、Fe2O3、PbO、CdO和稀硫酸反应生成Fe2+、Zn2+、Fe3+、PbSO4、Cd2+,所以滤渣1为未反应的SiO2和生成的PbSO4;氧化除杂时,通入氧气,使Fe2+转化为Fe3+,加入ZnO调节溶液的pH值,将Fe3+转化为Fe(OH)3而除去Fe3+,滤渣2为生成的Fe(OH)3;然后向溶液中加入Zn,Zn和Cd2+发生氧化还原生成Cd,然后过滤得到滤液,滤渣3为Cd;将滤液电解得到Zn。
A. 加入稀硫酸酸浸,FeS(未焙烧)、ZnO、Fe2O3、PbO、CdO和稀硫酸反应生成Fe2+、Zn2+、Fe3+、PbSO4、Cd2+,所以滤渣1为未反应的SiO2和生成的PbSO4;氧化除杂时,通入氧气,使Fe2+转化为Fe3+,加入ZnO调节溶液的pH值,将Fe3+转化为Fe(OH)3而除去Fe3+,滤渣2为生成的Fe(OH)3,A错误;
B. 闪锌矿主要含有ZnS,还含有SiO2和少量FeS、CdS、PbS杂质,焙烧过程中发生的主要反应有2ZnS+3O2![]() 2ZnO+2SO2,B正确;
2ZnO+2SO2,B正确;
C. Zn的金属性强于Cd,可以从溶液中将Cd置换出来,其离子反应方程式为:Zn+Cd2+=Zn2++Cd,C正确;
D. 氧化除杂时,通入氧气,使Fe2+转化为Fe3+,加入ZnO调节溶液的pH值,将Fe3+转化为Fe(OH)3而除去Fe3+,若不通入氧气,无法除去杂质Fe2+,D正确;
故答案为:A。

 计算高手系列答案
计算高手系列答案