��Ŀ����
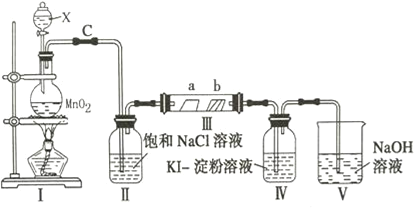
����Ŀ���⻯�(LiH)�ڸ���Ŀ��������ȶ����ڣ���ˮ������ҷ�Ӧ���ܹ�����ȼ�ա�ij��ѧ����С����ʹ������װ���Ʊ�LiH���塣����˵����ȷ����
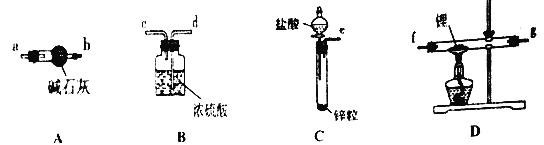
A. ��������װ�ð���������������˳��Ϊ��e��d��c��f��g��a��b(��g����Ҳ����)
B. ʵ�������õĽ���ﮱ�����ú����
C. �ڼ���D����ʯӢ��֮ǰ��Ӧ��ͨ��һ��ʱ���������ž�װ���ڵĿ���
D. ������еļ�ʯ�ҿ�������ˮCaCl2����
���𰸡�C
��������
������﮷�����Ӧ����LiH���Ʊ�LiH������Ҫ�Ʊ�������LiH�ڸ���Ŀ��������ȶ����ڣ���ˮ�����ܹ�����ȼ�գ������Ʊ��õ�������������﴿��������Cװ���Ʊ���������װ��A�еļ�ʯ�ҳ�ȥ�����е��Ȼ����ˮ������ͨ��װ��D�м��Ⱥ�﮷�Ӧ�����⻯ﮣ��������װ��B����ֹ�����е�ˮ�����Ͷ�����̼����װ��D�����ɵ��⻯﮷�����Ӧ��
A��������﮷�����Ӧ����LiH���Ʊ�LiH������Ҫ�Ʊ�������LiH�ڸ���Ŀ��������ȶ����ڣ���ˮ�����ܹ�����ȼ�գ������Ʊ��õ�������������﴿��������Cװ���Ʊ���������װ��A�еļ�ʯ�ҳ�ȥ�����е��Ȼ����ˮ������ͨ��װ��D�м��Ⱥ�﮷�Ӧ�����⻯ﮣ��������װ��B����ֹ�����е�ˮ�����Ͷ�����̼����װ��D�����ɵ��⻯﮷�����Ӧ��װ������˳��Ϊ��e��a��b��f��g��d����A������
B��ʵ�������õĽ���ﮱ�����ʯ���У���B����
C���ڼ���D����ʯӢ��֮ǰ��Ӧ��ͨ��һ��ʱ���������ž�װ���ڵĿ�������ֹ����ʱ�ȼ�գ�Ҳ��ֹ����������������ը��Ӧ����C��ȷ��
D����װ��A�еļ�ʯ�ҳ�ȥ�����е��Ȼ����ˮ������������еļ�ʯ�Ҳ���������ˮCaCl2���棬CaCl2����ȥHCl����D����
��ѡC��

����Ŀ��ij��ѧ��ȤС��Ҫ����к��ȵIJⶨ��
��1��ʵ�����ϱ��д�С�����ձ�����Ͳ����ĭ���ϡ���ĭ���ϰ塢��ͷ�ιܡ�0.5 mol��L-1���ᡢ0.55 mol��L-1NaOH��Һ,ʵ����ȱ�ٵIJ�����Ʒ��______��_______________�����Ǽ�¼��ʵ����������:
ʵ����Ʒ | ��Һ�¶� | �к��� | |||
t1 | t2 | ��H | |||
�� | 50 mL0.55 mol��L-1NaOH��Һ | 50 mL0.5mol��L-1HCl��Һ | 20 �� | 23.3 �� | |
�� | 50 mL0.55 mol��L-1NaOH��Һ | 50 mL0.5 mol��L-1 HCl��Һ | 20 �� | 23.5 �� | |
��֪:Q=cm(t2-t1),��Ӧ����Һ�ı�����cΪ4.18 kJ����-1��kg-1,�����ʵ��ܶȾ�Ϊ1 g��cm-3��
��2��NaOH������HCl�����Զ��ԭ����_________________________________��
��3������ʵ����д��NaOH��Һ��HCl��Һ��Ӧ���Ȼ�ѧ����ʽ: ___________________��
��4������KOH����NaOH,�Բⶨ���________(���������� ������)Ӱ��;���ô������HCl��ʵ��,�Բⶨ���__________(����������������)Ӱ�졣
��5������Һ��Ϻ�����������Һ_________________________________��
����Ŀ����1����һ�������°����������ܷ�����Ӧ���ɵ�����ˮ������4NH3(g)+3O2(g)=2N2(g)+6H2O(g) ��H
�������Ͽɵ��йصĻ�ѧ�������������£�
��ѧ�� | N��N | H��O | N��H | O=O |
E/ (kJ��mol��1) | 946 | 463 | 391 | 496 |
�ɴ˼���������Ӧ�ķ�Ӧ����H=___________kJ��mol��1��
��2����֪��N2(g)+O2(g)=2NO(g) K1
N2(g)+3H2(g)=2NH3(g) K2
2H2(g)+O2(g)=2H2O(g) K3
ע��K1��K2��K3�ֱ�Ϊ����������Ӧ��ƽ�ⳣ��
�ش��������⣺
�ٰ���������Ӧ(������̬ˮ)��ƽ�ⳣ��KΪ___________(��K1��K2��K3��ʾ)��
��һ�������£���4molNH3��5.2molO2������ݻ�Ϊ4L�ĺ����ܱ������з�����������Ӧ������10s��ﵽƽ�⣬���NO��Ũ��Ϊ0.4mol/L��0��10s�ڣ���NH3��ʾ�÷�Ӧ��ƽ����Ӧ����Ϊ___________��O2��ת����Ϊ___________(�ðٷ�����ʾ���ұ���С�����һλ)���÷�Ӧ��ƽ�ⳣ��Ϊ___________(�г�����ʽ����)��
����������Ӧ��һ�δﵽƽ��ʱ�����������������������£�ֻ�ǽ��������������һ�����ٶ���25s��ﵽ�µ�ƽ�⡣������ͼ�������߱�ʾ15~30s�������ϵ��NH3��Ũ����ʱ��仯�����ơ�__________

��3�������йظ÷�Ӧ��˵����ȷ����___________(����ĸ)��
A.���º��ݣ��ٳ���4molNH3��5.2molO2���ٴδﵽƽ��ʱ��NH3��ת��������
B.���º��ݣ��������ڵ��ܶȱ��ֲ���ʱ����Ӧ�ﵽ��ƽ��
C.����������ƽ��Ħ����������ʱ����Ӧ�ﵽ��ƽ��
D.��2v��(NO)=3v��(H2O)ʱ����Ӧ�ﵽ��ƽ��
��4����ҵ�ϳ��ð�ˮ����SO2��������(NH4)2SO3�����жϳ�����(NH4)2SO3��Һ������Բ�ͨ������˵���ж����ݣ�_______________________________________________________��(��֪��NH3��H2O��Kb=1.8��10��5��H2SO3��Ka1=1.3��10��2��Ka2=6.3��10��8)