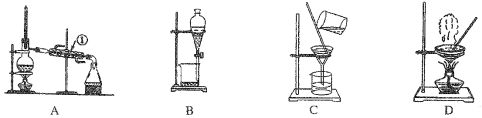
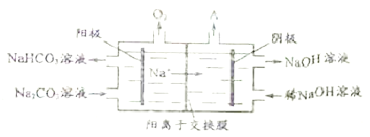
题目内容
【题目】药物Q适用于治疗高血压、心绞痛,可由有机物P和L制备。
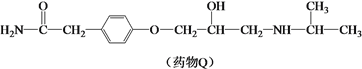
(1)有机物P的合成路线如下。

已知:![]() (R、R’、R”代表烃基或氢)
(R、R’、R”代表烃基或氢)
① A的分子式为C3H8O,其所含的官能团是_______。
② B的核磁共振氢谱只有一个吸收峰,其结构简式是_______。
③ 由D生成有机物P的反应类型是_______。
(2)有机物L的合成路线如下。
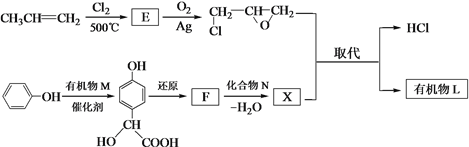
已知:![]()
① 生成E的化学方程式是_______。
② ![]() 与有机物M发生加成反应, M的结构简式为_______。
与有机物M发生加成反应, M的结构简式为_______。
③ F含羧基,化合物N是_______。
④ 生成有机物L的化学方程式是_______。
(3)以![]() 为起始原料合成聚合物甲的路线如下:
为起始原料合成聚合物甲的路线如下:
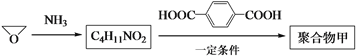
写出聚合物甲的结构简式:___________。
【答案】 羟基(或—OH) ![]() 加成反应(或还原反应)
加成反应(或还原反应) ![]()
![]()
![]()
![]()

【解析】(1)![]() 与水在催化剂作用下发生加成反应生成A,则A的分子式为C3H8O,结构简式为
与水在催化剂作用下发生加成反应生成A,则A的分子式为C3H8O,结构简式为![]() 或
或![]() ,A氧化生成B,B的核磁共振氢谱只有一个吸收峰,则B为
,A氧化生成B,B的核磁共振氢谱只有一个吸收峰,则B为![]() ,A为2-丙醇,根据信息,结合P的结构可知,D为
,A为2-丙醇,根据信息,结合P的结构可知,D为![]() 。
。
①A为![]() ,官能团是羟基,故答案为:羟基;
,官能团是羟基,故答案为:羟基;
② B为![]() ,故答案为:
,故答案为:![]() ;
;
③ 根据流程图,D(![]() )与氢气加成生成有机物P(
)与氢气加成生成有机物P(![]() ),故答案为:加成反应;
),故答案为:加成反应;
(2)根据流程图,CH3CH=CH2与氯气在500℃时发生甲基上的取代反应生成E,E氧化生成![]() ,则E为CH2ClCH=CH2;苯酚与M发生加成反应生成
,则E为CH2ClCH=CH2;苯酚与M发生加成反应生成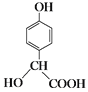 ,则M为
,则M为![]() ;根据Q(
;根据Q(![]() )由有机物P(
)由有机物P(![]() )和L制备,根据已知信息
)和L制备,根据已知信息![]() ,L中含有环氧乙烷的结构,则L为
,L中含有环氧乙烷的结构,则L为![]() ;X与
;X与![]() 反应生成L和氯化氢,则X为
反应生成L和氯化氢,则X为![]() ;F含羧基,则F为
;F含羧基,则F为![]() ,F为N生成X(
,F为N生成X(![]() ),则N为氨气。
),则N为氨气。
① CH3CH=CH2与氯气在500℃时发生甲基上的取代反应生成E(CH2ClCH=CH2),反应的化学方程式为![]() ,故答案为:
,故答案为:![]() ;
;
② 根据上述分析,![]() 与有机物M发生加成反应,M为
与有机物M发生加成反应,M为![]() ,故答案为:
,故答案为:![]() ;
;
③根据上述分析,化合物N是![]() ,故答案为:
,故答案为:![]() ;
;
④ 生成有机物L的化学方程式为![]() ,故答案为:
,故答案为:![]() ;
;
(3)根据![]() ,结合化学式C4H11NO2可知,2份
,结合化学式C4H11NO2可知,2份![]() 与氨气反应生成HOCH2CH2NHCH2CH2OH,HOCH2CH2NHCH2CH2OH与
与氨气反应生成HOCH2CH2NHCH2CH2OH,HOCH2CH2NHCH2CH2OH与![]() 发生缩聚反应生成聚合物甲,甲为
发生缩聚反应生成聚合物甲,甲为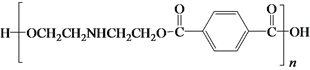 ,故答案为:
,故答案为: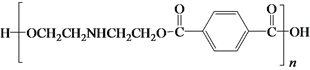 。
。

 名校课堂系列答案
名校课堂系列答案【题目】CH4、CO2和碳酸都是碳的重要化合物,实现碳及其化合物的相互转化,对开发新能源和降低碳排放意义重大。
(1)已知:①CH4(g)+H2O(g)![]() CO(g)+3H2(g) △H1=+206.1kJmol—1
CO(g)+3H2(g) △H1=+206.1kJmol—1
②2H2(g)+CO(g)![]() CH3OH(l) △H2=-128.3kJmol—1
CH3OH(l) △H2=-128.3kJmol—1
③2H2(g)+O2(g)=2H2O(g) △H3=-483.6kJmol—1
写出由甲烷和氧气合成液态甲醇的热化学方程式:_____________________。
(2)若利用反应①来制备氢气。为了探究温度、压强对反应①的影响,设计以下三组对比实验(温度为400℃或500℃,压强为101kPa或404kPa)。
实验序号 | 温度/℃ | 压强/kPa | CH4初始浓度/ mol·L—1 | H2O初始浓度/ mol·L—1 |
1 | 400 | 101 | 3.0 | 7.0 |
2 | T | 101 | 3.0 | 7.0 |
3 | 400 | P | 3.0 | 7.0 |
Ⅰ、实验1、实验2和实验3比较,反应开始时正反应速率最快的是_________;平衡时CH4的转化率最小的是_________。
Ⅱ、实验2和实验3相比,其平衡常数关系:K2______K3(填“>”、“<”或“=”)。
(3)科学家提出由CO2制取碳(C)的太阳能工艺如图1所示.
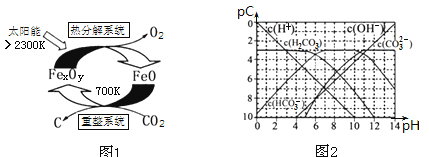
①“重整系统”发生的反应中n(FeO)∶n(CO2)=6∶1,则FexOy的化学式为______;
②“热分解系统”中每分解l mol FexOy,同时生成标准状况下气体体积为_______。
(4)pC类似pH,是指极稀溶液中的溶质浓度的常用负对数值。如某溶液中溶质的浓度为1×10—2molL—1,则该溶液中溶质的pC=﹣lg(1×10—2)=2。上图2为25℃时H2CO3溶液的pC﹣pH图。请回答下列问题:
①
②在8<pH<10时,溶液中HCO3—的pC值不随着pH增大而减小的原因是____;
③求H2CO3一级电离平衡常数的数值Ka1= _______________。