题目内容
下列各组物质不属于同分异构体的是( )
| A、1,3-丁二烯和环丁烷 |
| B、邻氯甲苯和对氯甲苯 |
| C、2-甲基丁烷和戊烷 |
| D、2,2-二甲基丙醇和2-甲基丁醇 |
考点:有机化合物的异构现象
专题:同分异构体的类型及其判定
分析:根据分子式相同,结构不同的化合物互为同分异构体来判断.
解答:
解:A.1,3-丁二烯的分子式为C4H6,环丁烷的分子式为C4H8,分子式不相同,不是同分异构体,故A选;
B.邻氯甲苯和对氯甲苯都为C7H7Cl,分子式相同,结构不同的化合物,互为同分异构体,故B不选;
C.2-甲基丁烷和戊烷的分子式都为C5H12,是分子式相同,结构不同的化合物,互为同分异构体,故C不选;
D.2,2-二甲基丙醇和2-甲基丁醇的分子式都为C5H120,是分子式相同,结构不同的化合物,互为同分异构体,故D不选.
故选A.
B.邻氯甲苯和对氯甲苯都为C7H7Cl,分子式相同,结构不同的化合物,互为同分异构体,故B不选;
C.2-甲基丁烷和戊烷的分子式都为C5H12,是分子式相同,结构不同的化合物,互为同分异构体,故C不选;
D.2,2-二甲基丙醇和2-甲基丁醇的分子式都为C5H120,是分子式相同,结构不同的化合物,互为同分异构体,故D不选.
故选A.
点评:本题考查同分异构体的概念与区别,难度不大,关键是根据名称写出分子式进行判断.

练习册系列答案
相关题目
下列有关物质的性质和该性质的应用均正确的是( )
| A、常温下浓硝酸能使铝发生钝化,可在常温下用铝制贮藏贮运浓硝酸 |
| B、二氧化硅不与任何酸反应,可用石英制造耐酸容器 |
| C、ClO2具有还原性,可用于对自来水的杀菌消毒 |
| D、铜的金属活泼性比铁的差,所以氯化铁溶液不能溶解铜 |
下列反应的离子方程式正确的是( )
| A、钠与硫酸铜溶液反应:2Na++Cu═Cu2++2Na+ |
| B、铁跟稀硫酸反应:2Fe+6H+═2Fe3++3H2↑ |
| C、向CaCl2溶液中通入CO2气体:Ca2++CO2+H2O═CaCO3↓+2H+ |
| D、将氯气通入足量的氯化亚铁溶液中:Cl2+2Fe2+═2Cl-+2Fe3+ |
关于实验室制取乙烯的说法不正确的是( )
| A、温度计插入到反应物液面以下 |
| B、生成的乙烯混有刺激性气味的气体 |
| C、反应过程中溶液的颜色会逐渐变黑 |
| D、加热时要注意使温度缓慢上升至170℃ |
下列说法不正确的是( )
| A、某烷烃主链4个碳原子数的同分异构体有2种,则与其碳原子个数相同的且主链4个碳原子的单烯烃有4种 |
| B、(CH3)2C(OH)CH2CH3的名称为:2-甲基-2-羟基丁烷 |
C、1mol有机物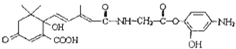 与NaOH溶液反应,最多消耗5mol NaOH 与NaOH溶液反应,最多消耗5mol NaOH |
D、1mol β-紫罗兰酮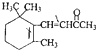 与1mol Br2发生加成反应可得到3种不同产物 与1mol Br2发生加成反应可得到3种不同产物 |
下列给定条件的各组离子或分子一定能大量共存的是( )
| A、84消毒液:H+、Cl-、K+、SO42- |
| B、透明的KCl溶液:Na+、Cu2+、SO42-、NO3- |
| C、王水中:Ag+、NO3-、Cl-、Au |
| D、空气中:N2、CH4、CO、C6H5OH |
下列各表述与示意图一致的是( )
A、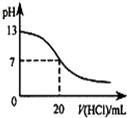 如图表示25℃时,用0.1mol?L-1盐酸滴定20mL 0.1mol?L-1 NaOH溶液,溶液的pH随加入酸体积的变化 |
B、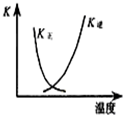 图中曲线表示反应2SO2(g)+O2(g)?2SO3(g)△H<0,正、逆反应的平衡常数K随温度的变化 |
C、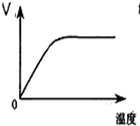 如图表示淀粉在淀粉酶作用下水解速率随温度的变化 |
D、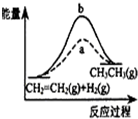 图中a、b曲线分别表示反应CH2=CH2(g)+H2(g)→CH3CH3(g)△H<0使用(a)和未使用(b)催化剂时,反应过程中的能量变化 |
X、Y、Z、W、R是5种短周期元素,其原子序数依次增大.X是周期表中原子半径最小的元素,Y原子最外层电子数是次外层电子数的3倍,Z、W、R处于同一周期,R与Y处于同一族,Z、W原子的核外电子数之和与Y、R原子的核外电子数之和相等.下列说法正确的是( )
| A、物质A由Z与Y两种元素组成,则0.5mol物质A中含有的离子数约为9.03×1023 |
| B、元素Y、Z、W形成的离子具有相同电子层结构,其离子半径依次增大 |
| C、元素Z、R的氧化物的水化物之间相互反应生成的盐溶液呈中性或碱性 |
| D、元素Y、R分别与元素X形成的化合物的沸点:XmY<XmR |
 如图是某同学利用注射器设计的简易实验装置.甲管中注入10mL
如图是某同学利用注射器设计的简易实验装置.甲管中注入10mL