题目内容
下列反应的离子方程式正确的是( )
| A、钠与硫酸铜溶液反应:2Na++Cu═Cu2++2Na+ |
| B、铁跟稀硫酸反应:2Fe+6H+═2Fe3++3H2↑ |
| C、向CaCl2溶液中通入CO2气体:Ca2++CO2+H2O═CaCO3↓+2H+ |
| D、将氯气通入足量的氯化亚铁溶液中:Cl2+2Fe2+═2Cl-+2Fe3+ |
考点:离子方程式的书写
专题:离子反应专题
分析:A.钠在溶液中无法置换出金属铜,反应实质是钠先与水反应生成氢氧化钠和氢气,然后氢氧化钠与硫酸铜反应生成氢氧化铜沉淀;
B.铁与稀硫酸反应生成的是硫酸亚铁,不会生成铁离子;
C.氯化钙溶液与二氧化碳不发生反应,无法形成反应的离子方程式;
D.氯气与氯化亚铁溶液反应,亚铁离子被氯气氧化成铁离子.
B.铁与稀硫酸反应生成的是硫酸亚铁,不会生成铁离子;
C.氯化钙溶液与二氧化碳不发生反应,无法形成反应的离子方程式;
D.氯气与氯化亚铁溶液反应,亚铁离子被氯气氧化成铁离子.
解答:
解:A.钠与硫酸铜溶液反应生成氢氧化铜沉淀、硫酸钠和氢气,正确的离子方程式为:2Na+2H2O+Cu2+═H2↑+2Na++Cu(OH)2↓,故A错误;
B.Fe跟稀硫酸反应生成硫酸亚铁和氢气,正确的离子方程式为:Fe+2H+═Fe2++H2↑,故B错误;
C.氯化钙溶液不与二氧化碳发生反应,无法形成离子方程式,故C错误;
D.氯气通入足量的氯化亚铁溶液中,反应生成氯化铁,反应的离子方程式为:Cl2+2Fe2+═2Cl-+2Fe3+,故D正确;
故选D.
B.Fe跟稀硫酸反应生成硫酸亚铁和氢气,正确的离子方程式为:Fe+2H+═Fe2++H2↑,故B错误;
C.氯化钙溶液不与二氧化碳发生反应,无法形成离子方程式,故C错误;
D.氯气通入足量的氯化亚铁溶液中,反应生成氯化铁,反应的离子方程式为:Cl2+2Fe2+═2Cl-+2Fe3+,故D正确;
故选D.
点评:本题考查了离子方程式的正误判断,该题是高考中的高频题,为中等难度的试题,注意掌握离子方程式的书写原则,明确离子方程式正误判断常用方法:检查反应能否发生,检查反应物、生成物是否正确,检查各物质拆分是否正确,如难溶物、弱电解质等需要保留化学式,检查是否符合守恒关系(如:质量守恒和电荷守恒等)、检查是否符合原化学方程式等.

练习册系列答案
 各地期末复习特训卷系列答案
各地期末复习特训卷系列答案 小博士期末闯关100分系列答案
小博士期末闯关100分系列答案
相关题目
下列叙述中能证明次氯酸是一种弱酸的是( )
| A、次氯酸不稳定,易分解 |
| B、次氯酸是一种强氧化剂 |
| C、次氯酸钙能与碳酸作用生成碳酸钙和次氯酸 |
| D、次氯酸能使染料和有机色质褪色 |
下列表达方式错误的是( )
A、碳-12原子
| ||
B、氟化钠的电子式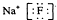 | ||
| C、硫离子的核外电子排布式 1s22s22p63s23p4 | ||
D、甲烷的电子式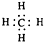 |
下列说法中正确的是( )
A、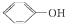 与 与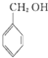 互为同系物 互为同系物 |
| B、乙醇和乙醚互为同分异构体 |
| C、可用浓溴水来区分乙醇和苯酚 |
| D、乙醇、乙二醇、丙三醇互为同系物 |
100mL浓度为2mol?L-1的盐酸跟过量的锌片反应,为加快反应速率,又不影响生成氢气的总量,可采用的方法是( )
| A、加入适量的6mol?L-1的盐酸 |
| B、加入适量的氯化钠溶液或降温 |
| C、加入适量CH3COOK溶液 |
| D、加入2滴氯化铜溶液或碳粉 |
如图是化学实验常用装置之一,若气体从右管进入,可用来收集的气体是( )
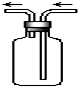

| A、NO |
| B、NO2 |
| C、NH3 |
| D、SO2 |
下列各组物质不属于同分异构体的是( )
| A、1,3-丁二烯和环丁烷 |
| B、邻氯甲苯和对氯甲苯 |
| C、2-甲基丁烷和戊烷 |
| D、2,2-二甲基丙醇和2-甲基丁醇 |
下列操作中不正确的是( )
| A、铁粉中混有铝粉:加入过量烧碱溶液充分反应、过滤 |
| B、检验SO2中是否含CO2:先通入到饱和NaHCO3溶液中除SO2,再通入到澄清石灰水中 |
| C、NaHCO3溶液中混有少量Na2CO3:往该溶液中通入过量CO2气体 |
| D、NaCl溶液中混有少量I2:加入适量CCl4,振荡,静置,分液 |