题目内容
MnO2、KMnO4等是中学化学中的常用试剂。请回答下列问题:
(1)MnO2在H2O2分解反应中作催化剂。若将MnO2加入酸化的H2O2溶液中,MnO2 溶解产生Mn2+,反应的离子方程式是 。
(2)用MnO2制KMnO4的工艺流程如图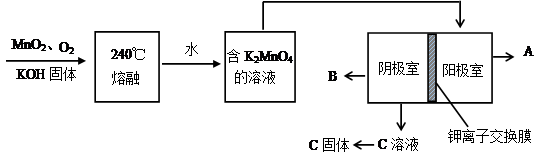
电解池中两极材料均为碳棒,在水或酸性溶液中K2MnO4发生歧化而变成MnO2和KMnO4。
①写出240℃熔融时发生反应的化学方程式 ,投料时必须满足n(KOH):n(MnO2) 。
②阳极的电极反应为 。
③B物质是 (写化学式,下同),可以循环使用的物质是 。
④钾离子交换膜的一种材料是聚丙烯酸钾(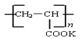 ),聚丙烯酸钾单体的结构简式为 。
),聚丙烯酸钾单体的结构简式为 。
⑤上述制得的KMnO4产品0.165 g,恰好与0.335 g经硫酸酸化的Na2C2O4反应完全,该KMnO4的
纯度是 (精确到0.1%)。
(1)MnO2 + 2H+ + H2O2 = Mn2+ + O2 ↑+ 2H2O
(2)①2MnO2 + O2 + 4KOH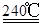 2K2MnO4 + 2H2O ,大于(或 >)2 : 1
2K2MnO4 + 2H2O ,大于(或 >)2 : 1
② MnO42- - e- = MnO4- ③ H2,KOH固体 ④ CH2="CHCOOK" ⑤ 95.8%
解析试题分析:(1)根据题意,结合电荷守恒、原子守恒、电子守恒,可得方程式为:MnO2 + 2H+ + H2O2 = Mn2+ + O2 ↑+ 2H2O。(2)①在240℃熔融时MnO2、O2、KOH发生氧化还原反应,根据质量守恒定律和电子守恒的知识可知发生该反应的化学方程式为:2MnO2 + O2 + 4KOH 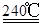 2K2MnO4 + 2H2O。由方程式可知在投料时必须满足n(KOH):n(MnO2)=2:1,为了使MnO2充分发生反应,KOH必须过量。因此二者的物质的量的比要大于2:1. ②由题意知道K2MnO4应该在阳极发生氧化反应,失去电子,被氧化为KMnO4。所以阳极的电极反应为MnO42- - e- = MnO4- 。③在阴极发生反应:2H2O+2e-=H2↑+2OH-.所以B物质是H2。根据电极反应式可以看出在此过程中可以循环的物质为KOH。④钾离子交换膜的一种材料是聚丙烯酸钾 。该物质为丙烯酸钾发生加聚反应得到的,其结构简式为 CH2=CHCOOK。⑤Na2C2O4与酸性KMnO4溶液发生反应的方程式为:5Na2C2O4+2KMnO4+8H2SO4=5Na2SO4+K2SO4+2MnSO4 +10CO2↑+8H2O。n(Na2C2O4)="0.335" g÷134g/mol=0.0025mol;则根据反应方程式可知消耗的KMnO4的物质的量为0.0025mol×2/5=0.001mol.其质量为0.001mol×158g/mol=0.158g.所以该KMnO4的纯度是0.158g÷0.165 g×100%=95.8%.
2K2MnO4 + 2H2O。由方程式可知在投料时必须满足n(KOH):n(MnO2)=2:1,为了使MnO2充分发生反应,KOH必须过量。因此二者的物质的量的比要大于2:1. ②由题意知道K2MnO4应该在阳极发生氧化反应,失去电子,被氧化为KMnO4。所以阳极的电极反应为MnO42- - e- = MnO4- 。③在阴极发生反应:2H2O+2e-=H2↑+2OH-.所以B物质是H2。根据电极反应式可以看出在此过程中可以循环的物质为KOH。④钾离子交换膜的一种材料是聚丙烯酸钾 。该物质为丙烯酸钾发生加聚反应得到的,其结构简式为 CH2=CHCOOK。⑤Na2C2O4与酸性KMnO4溶液发生反应的方程式为:5Na2C2O4+2KMnO4+8H2SO4=5Na2SO4+K2SO4+2MnSO4 +10CO2↑+8H2O。n(Na2C2O4)="0.335" g÷134g/mol=0.0025mol;则根据反应方程式可知消耗的KMnO4的物质的量为0.0025mol×2/5=0.001mol.其质量为0.001mol×158g/mol=0.158g.所以该KMnO4的纯度是0.158g÷0.165 g×100%=95.8%.
考点:考查化学方程式、离子方程式的书写、电解池的化学反应原理、聚合物与单体的相互转化、物质的转化率的计算的知识。

Ⅰ.磷、硫元素的单质和化合物应用广泛。
(1)磷元素的原子结构示意图是 。
(2)磷酸钙与焦炭、石英砂混合,在电炉中加热到1 500 ℃生成白磷,反应为:
2Ca3(PO4)2+6SiO2 6CaSiO3+P4O10
6CaSiO3+P4O10
10C+P4O10 P4+10CO
P4+10CO
每生成1 mol P4时,就有 mol电子发生转移。
(3)硫代硫酸钠(Na2S2O3)是常用的还原剂。在维生素C(化学式C6H8O6)的水溶液中加入过量I2溶液,使维生素C完全氧化,剩余的I2用Na2S2O3溶液滴定,可测定溶液中维生素C的含量。发生的反应为:
C6H8O6+I2 C6H6O6+2H++2I-
C6H6O6+2H++2I-
2S2 +I2
+I2 S4
S4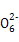 +2I-
+2I-
在一定体积的某维生素C溶液中加入a mol/L I2溶液V1 mL,充分反应后,用Na2S2O3溶液滴定剩余的I2,消耗b mol/L Na2S2O3溶液V2 mL。该溶液中维生素C的物质的量是 mol。
(4)在酸性溶液中,碘酸钾(KIO3)和亚硫酸钠可发生如下反应:
2I +5S
+5S +2H+
+2H+ I2+5S
I2+5S +H2O
+H2O
生成的碘可以用淀粉溶液检验,根据反应溶液出现蓝色所需的时间来衡量该反应的速率。
某同学设计实验如下表所示:
| | 0.01 mol/LKIO3酸性溶液(含淀粉)的体积/mL | 0.01 mol/LNa2SO3溶液的体积/mL | H2O的体积/mL | 实验温度/℃ | 溶液出现蓝色时所需时间/s |
| 实验1 | 5 | V1 | 35 | 25 | |
| 实验2 | 5 | 5 | 40 | 25 | |
| 实验3 | 5 | 5 | V2 | 0 | |
该实验的目的是 ;表中V2= mL。
Ⅱ.稀土元素是宝贵的战略资源,我国的蕴藏量居世界首位。
(5)铈(Ce)是地壳中含量最高的稀土元素。在加热条件下CeCl3易发生水解,无水CeCl3可用加热CeCl3·6H2O和NH4Cl固体混合物的方法来制备。其中,NH4Cl的作用是 。
(6)在某强酸性混合稀土溶液中加入H2O2,调节pH≈3,Ce3+通过下列反应形成Ce(OH)4沉淀得以分离。完成反应的离子方程式:
Ce3++H2O2+H2O
 Ce(OH)4↓+ 。
Ce(OH)4↓+ 。  Ag2O2↓+2KNO3+2K2SO4+2H2O
Ag2O2↓+2KNO3+2K2SO4+2H2O

 8Cu+4FeO+2Fe2O3+16SO2
8Cu+4FeO+2Fe2O3+16SO2