题目内容
14.标准状况下,Na2O2与2.24LCO2反应,生成氧气的物质的量为0.05mol,转移电子个数为0.1NA,当转移4mole-时,消耗CO2体积为89.6L,生成氧气的物质的量为2mol.分析 发生反应:2CO2+2Na2O2=2Na2CO3+O2 ,标况下n(CO2)=$\frac{2.24L}{22.4L/mol}$=0.1mol,根据二氧化碳和氧气关系式计算生成氧气物质的量;该反应中如果有2mol二氧化碳反应,有2mol电子转移,据此计算转移电子个数;根据转移电子和二氧化碳、氧气之间关系式计算消耗二氧化碳体积、生成氧气物质的量.
解答 解:发生反应:2CO2+2Na2O2=2Na2CO3+O2 ,标况下n(CO2)=$\frac{2.24L}{22.4L/mol}$=0.1mol,根据二氧化碳和氧气关系式知,生成氧气物质的量=$\frac{0.1mol}{2}×1$=0.05mol;该反应中如果有2mol二氧化碳反应,有2mol电子转移,则有0.1mol二氧化碳参加反应转移电子0.1mol,所以转移电子数=0.1NA;
反应中如果有2mol二氧化碳反应,有2mol电子转移,则当转移4mole-时,消耗CO2物质的量为4mol,其体积=4mol×22.4L/mol=89.6L;
反应中有2mol电子转移时生成1mol氧气,所以当转移4mole-时,生成氧气的物质的量是2mol,
故答案为:0.05mol;0.1NA;89.6;2mol.
点评 本题考查物质的量有关计算,明确各个物理量关系式是解本题关键,注意该反应中过氧化钠既是氧化剂又是还原剂,题目难度不大.

练习册系列答案
相关题目
5. 1913年,德国化学家哈伯实现了合成氨的工业化生产,被称作解救世界粮食危机的化学天才.现将lmolN2和3molH2投入1L的密闭容器,在一定条件下,利用反应:
1913年,德国化学家哈伯实现了合成氨的工业化生产,被称作解救世界粮食危机的化学天才.现将lmolN2和3molH2投入1L的密闭容器,在一定条件下,利用反应: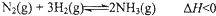 模拟哈伯合成氨的工业化生产.当改变某一外界条件(温度或压强)时,NH3的体积分数ψ(NH3)变化趋势如图所示.
模拟哈伯合成氨的工业化生产.当改变某一外界条件(温度或压强)时,NH3的体积分数ψ(NH3)变化趋势如图所示.
回答下列问题:
(1)已知:①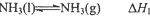
②
则反应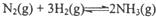 的△H=2△H1+△H2,(用含△H1、△H2的代数式表示).
的△H=2△H1+△H2,(用含△H1、△H2的代数式表示).
(2)合成氨的平衡常数表达式为$\frac{{c}^{2}(N{H}_{3})}{c({N}_{2})×{c}^{3}({H}_{2})}$,平衡时,M点NH3的体积分数为10%,则N2的转化率为18%(保留两位有效数字)
(3)X轴上a点的数值比b点小(填“大”或“小”).上图中,Y轴表示温度(填“温度”或“压强”),判断的理由是随Y值增大,φ(NH3)减小,平衡N2(g)+3H2(g)?2NH3(g)△H<0向逆反应方向移动,故Y为温度.
(4)若将1mol N2和3mol H2分别投入起始容积为1L的密闭容器中,实验条件和平衡时的相关数据如表所示:
下列判断正确的是AB.
A.放出热量:Ql<Q2 B.N2的转化率:I>III
C.平衡常数:II>I D.达平衡时氨气的体积分数:I>II
(5)下列能提高N2的转化率的是C
A.升高温度 B.恒容体系中通入N2气体
C.分离出NH3 D.通入稀有气体He,使体系压强增大到原来的5倍
(6)常温下,向VmL amoI.L-l的稀硫酸溶液中滴加等体积bmol.L-l 的氨水,恰好使混合溶液呈中性,此时溶液中c(NH4+)>c(S042-)(填“>”、“<”或“=”).
(7)利用氨气设计一种环保燃料电池,一极通入氨气,另一极通入空气,电解质是掺杂氧化钇(Y2O3)的氧化锆(ZrO2)晶体,它在熔融状态下能传导O2-.写出负极的电极反应式2NH3+3O2--6e-=N2+3H2O.
 1913年,德国化学家哈伯实现了合成氨的工业化生产,被称作解救世界粮食危机的化学天才.现将lmolN2和3molH2投入1L的密闭容器,在一定条件下,利用反应:
1913年,德国化学家哈伯实现了合成氨的工业化生产,被称作解救世界粮食危机的化学天才.现将lmolN2和3molH2投入1L的密闭容器,在一定条件下,利用反应: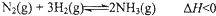 模拟哈伯合成氨的工业化生产.当改变某一外界条件(温度或压强)时,NH3的体积分数ψ(NH3)变化趋势如图所示.
模拟哈伯合成氨的工业化生产.当改变某一外界条件(温度或压强)时,NH3的体积分数ψ(NH3)变化趋势如图所示.回答下列问题:
(1)已知:①
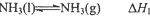
②

则反应
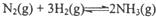 的△H=2△H1+△H2,(用含△H1、△H2的代数式表示).
的△H=2△H1+△H2,(用含△H1、△H2的代数式表示).(2)合成氨的平衡常数表达式为$\frac{{c}^{2}(N{H}_{3})}{c({N}_{2})×{c}^{3}({H}_{2})}$,平衡时,M点NH3的体积分数为10%,则N2的转化率为18%(保留两位有效数字)
(3)X轴上a点的数值比b点小(填“大”或“小”).上图中,Y轴表示温度(填“温度”或“压强”),判断的理由是随Y值增大,φ(NH3)减小,平衡N2(g)+3H2(g)?2NH3(g)△H<0向逆反应方向移动,故Y为温度.
(4)若将1mol N2和3mol H2分别投入起始容积为1L的密闭容器中,实验条件和平衡时的相关数据如表所示:
| 容器编号 | 实验条件 | 平衡时反应中的能量变化 |
| Ⅰ | 恒温恒容 | 放热Q1kJ |
| Ⅱ | 恒温恒压 | 放热Q2kJ |
| Ⅲ | 恒容绝热 | 放热Q3kJ |
A.放出热量:Ql<Q2 B.N2的转化率:I>III
C.平衡常数:II>I D.达平衡时氨气的体积分数:I>II
(5)下列能提高N2的转化率的是C
A.升高温度 B.恒容体系中通入N2气体
C.分离出NH3 D.通入稀有气体He,使体系压强增大到原来的5倍
(6)常温下,向VmL amoI.L-l的稀硫酸溶液中滴加等体积bmol.L-l 的氨水,恰好使混合溶液呈中性,此时溶液中c(NH4+)>c(S042-)(填“>”、“<”或“=”).
(7)利用氨气设计一种环保燃料电池,一极通入氨气,另一极通入空气,电解质是掺杂氧化钇(Y2O3)的氧化锆(ZrO2)晶体,它在熔融状态下能传导O2-.写出负极的电极反应式2NH3+3O2--6e-=N2+3H2O.
3.二甲醚是一种重要的清洁燃料,也可替代氟利昂作制冷剂等,对臭氧层无破坏作用.工业上可利用煤的气化产物(水煤气)合成二甲醚(CH3OCH3).
请回答下列问题:
(1)利用水煤气合成二甲醚的三步反应如下:(甲醇:CH3OH)
①2H2(g)+CO(g)═CH3OH(g);△H=-90.8kJ•mol-1
②2CH3OH(g)═CH3OCH3(g)+H2O(g);△H=-23.5kJ•mol-1
③CO(g)+H2O(g)═CO2(g)+H2(g);△H=-41.3kJ•mol-1
则利用水煤气合成二甲醚的总反应的热化学方程式为3H2(g)+3CO(g)?CH3OCH3(g)+CO2(g)△H=-246.4kJ•mol-1.
一定条件下的密闭容器中,该总反应达到平衡,要提高CO的转化率,可以采取的措施是ce(填字母代号).
a.高温高压 b.加入催化剂 c.减少CO2的浓度
d.增加CO的浓度 e.分离出二甲醚
(2)、已知反应②2CH3OH(g)═CH3OCH3(g)+H2O(g)某温度下的平衡常数为400.此温度下,在密闭容器中加入CH3OH,反应到某时刻测得各组分的浓度如下:
①比较此时正、逆反应速率的大小:v正> v逆 (填“>”、“<”或“=”).
②若加入CH3OH后,经10min反应达到平衡,此时c(CH3OH)=0.04mol/L;该时间内反应速率v(CH3OH)=0.16 mol/(L•min).
请回答下列问题:
(1)利用水煤气合成二甲醚的三步反应如下:(甲醇:CH3OH)
①2H2(g)+CO(g)═CH3OH(g);△H=-90.8kJ•mol-1
②2CH3OH(g)═CH3OCH3(g)+H2O(g);△H=-23.5kJ•mol-1
③CO(g)+H2O(g)═CO2(g)+H2(g);△H=-41.3kJ•mol-1
则利用水煤气合成二甲醚的总反应的热化学方程式为3H2(g)+3CO(g)?CH3OCH3(g)+CO2(g)△H=-246.4kJ•mol-1.
一定条件下的密闭容器中,该总反应达到平衡,要提高CO的转化率,可以采取的措施是ce(填字母代号).
a.高温高压 b.加入催化剂 c.减少CO2的浓度
d.增加CO的浓度 e.分离出二甲醚
(2)、已知反应②2CH3OH(g)═CH3OCH3(g)+H2O(g)某温度下的平衡常数为400.此温度下,在密闭容器中加入CH3OH,反应到某时刻测得各组分的浓度如下:
| 物质 | CH3OH | CH3OCH3 | H2O |
| 浓度/(mol•L-1) | 0.44 | 0.6 | 0.6 |
②若加入CH3OH后,经10min反应达到平衡,此时c(CH3OH)=0.04mol/L;该时间内反应速率v(CH3OH)=0.16 mol/(L•min).
