题目内容
【题目】某同学设计如下实验装置用于制取纯净的无水FeCl3.
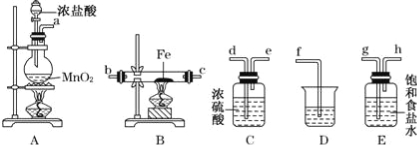
(1)图中盛放浓盐酸的实验仪器的名称为 ,A中发生反应的化学方程式为
(2)各装置的正确连接顺序为:a → → → → → → c → (填字母代号),
(3)装置E的作用是 ,装置C的作用是 。
(4)装置D中所发生反应的离子方程式为 .
(5)装置A中,如果反应产生氯气的体积为2.24L(标准状况),则反应中被氧化的HCl的质量为 ___________。
【答案】(1)分液漏斗;MnO2+4HCl(浓) ![]() MnCl2+Cl2↑+2H2O;
MnCl2+Cl2↑+2H2O;
(2)a →g→h→d→e→b→c→f;
(3)除去氯气中的HCl;干燥Cl2;
(4)Cl2+H2O![]() H++Cl-+HClO;(5)7.3g。
H++Cl-+HClO;(5)7.3g。
【解析】
试题分析:该实验目的是用Cl2和Fe反应制取FeCl3 固体,实验室用浓盐酸和MnO2加热制取Cl2,因为要制取纯净干燥的FeCl3,所以生成的Cl2必须是干燥、纯净的,浓盐酸、水都具有挥发性,所以生成的Cl2中含有HCl、H2O,用饱和食盐水除去HCl、用浓硫酸干燥Cl2,氯气有毒,不能直接排空,应该用碱液吸收Cl2。(1)图中盛放浓盐酸的实验仪器的名称为分液漏斗,实验室用浓盐酸和MnO2加热制取Cl2,二者反应生成氯化锰、氯气和水,反应方程式为MnO2+4HCl(浓) ![]() MnCl2+Cl2↑+2H2O;(2)各装置的正确连接顺序为气体制备装置、洗气装置、干燥装置、氯化铁制备装置、尾气处理装置,所以其连接顺序是a→g→h→d→e→b→c→f;(3)装置E的作用是吸收挥发出的HCl,装置C的作用是干燥气体,防止得不到干燥的氯化铁,故答案为:除去氯气中的氯化氢;干燥氯气;(4)装置D中氯气和水反应生成盐酸、次氯酸和水,反应的离子方程式为Cl2+H2O
MnCl2+Cl2↑+2H2O;(2)各装置的正确连接顺序为气体制备装置、洗气装置、干燥装置、氯化铁制备装置、尾气处理装置,所以其连接顺序是a→g→h→d→e→b→c→f;(3)装置E的作用是吸收挥发出的HCl,装置C的作用是干燥气体,防止得不到干燥的氯化铁,故答案为:除去氯气中的氯化氢;干燥氯气;(4)装置D中氯气和水反应生成盐酸、次氯酸和水,反应的离子方程式为Cl2+H2O![]() H++Cl-+HClO;(5)装置A中,如果反应产生氯气的体积为2.24L(标准状况),其物质的量n(Cl2)=2.24L÷22.4L/mol=0.1mol,根据Cl原子守恒计算反应中被氧化的n(HCl)=2n(Cl2)=2×0.1mol=0.2mol,被氧化HCl的质量是m(HCl)=n·M=0.2mol×36.5g/mol=7.3g。
H++Cl-+HClO;(5)装置A中,如果反应产生氯气的体积为2.24L(标准状况),其物质的量n(Cl2)=2.24L÷22.4L/mol=0.1mol,根据Cl原子守恒计算反应中被氧化的n(HCl)=2n(Cl2)=2×0.1mol=0.2mol,被氧化HCl的质量是m(HCl)=n·M=0.2mol×36.5g/mol=7.3g。

 阅读快车系列答案
阅读快车系列答案