题目内容
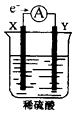
【题目】工业上合成甲醇的反应为:CO(g)+2H2(g)CH3OH(g)△H<0.500℃,5MPa条件下,将0.20mol CO与0.58mol H2的混合气体充入2L恒容密闭容器发生反应,反应过程中甲醇的物质的量浓度随时间的变化如图所示
(1)利用△H﹣T△S判断,该反应在条件下自发进行(填“高温”“低温”、或“任何温度”).
(2)计算500℃时该反应的平衡常数K= . CO 的平衡转化率为 .
(3)下列措施可增大甲醇产率的是 . A.压缩容器体积 B.将CO(g)从体系中分离
C.充入He,使体系总压强增大 D.再充入0.20mol CO和0.58mol H2
(4)可判断可逆反应达到平衡状态的依据是 . A.v正(CO)=2v逆(H2)
B.混合气体的密度不变
C.混合气体的平均相对分子质量不变
D.容器中CO、H2、CH3OH的物质的量之比为1:2:1
E.混合气体压强不再随时间变化而变化
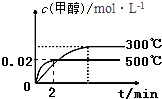
(5)若其它条件不变,使反应在300℃下进行,在上图中作出甲醇的物质的量浓度随时间的变化的示意图. 
【答案】
(1)低温
(2)4;20%
(3)A、D
(4)C、D
(5)
【解析】解:(1)CO(g)+2H2(g)CH3OH(g)△H<0,300℃,该反应的反应物有3mol气体,生成物有1mol气体,所以△S<0,反应自发进行△H﹣T△S<0,故低温下满足△H﹣T△S<0, 所以答案是:低温;(2)500℃,5MPa条件下,将0.20mol CO与0.58mol H2的混合气体充入2L恒容密闭容器发生反应,图像中达到平衡状态甲醇浓度为0.02mol/L,
CO(g)+ | 2H2(g) | CH3OH(g) | △H<0 | ||
起始量(mol/L) | 0.10 | 0.29 | 0 | ||
变化量(mol/L) | 0.02 | 0.04 | 0.02 | ||
平衡量(mol/L) | 0.08 | 0.25 | 0.02 |
平衡常数K= ![]() =v=4,
=v=4,
CO转化率= ![]() ×100%=
×100%= ![]() =20%,
=20%,
所以答案是:4,20%;(3)A、对于反应CO(g)+2H2(g)CH3OH(g),反应物气体体积大于生成物,压缩容器体积时,压强增大,平衡正向移动,可增加甲醇产率,A正确; B、分离出CO,平衡逆向移动可减少甲醇产率,故B错误; C、充入He,不影响各气体的分压,平衡不移动,不能增加甲醇产率,故C错误; D、体积不变,再充入0.20mol CO和0.58mol H2反应物气体,平衡正向移动,可增加甲醇产率,故D正确.故选AD;所以答案是:AD;(4)可逆反应达到平衡状态的依据是正逆反应速率相同,CO(g)+2H2(g)CH3OH(g)△H<0,反应是气体体积较小的放热反应, A.2v正(CO)=v逆(H2)说明氢气正逆反应速率相同,反应达到平衡状态,v正(CO)=2v逆(H2)不能说明反应达到平衡状态,故A错误; B.反应前后气体质量不变,容器体积不变,反应过程中密度不变,混合气体的密度不变不能说明反应达到平衡,故B错误; C.反应前后气体物质的量减小,质量守恒,混合气体的平均相对分子质量增大,混合气体的平均相对分子质量不变说明反应达到平衡状态,故C正确; D.容器中CO、H2、CH3OH的物质的量之比为1:2:1,符合反应之比,但不能说明正逆反应速率相同,故D错误; E.发邀请函气体物质的量发生变化,当混合气体压强不再随时间变化而变化说明反应达到平衡状态,故E正确;所以答案是:CE;(5)温度降低,反应速率减慢,达到平衡时间长.正反应放热,降温时平衡正向移动,平衡时甲醇浓度比500℃高,可得右图:  ,所以答案是:
,所以答案是:  .
.
【考点精析】通过灵活运用反应热和焓变和化学平衡状态本质及特征,掌握在化学反应中放出或吸收的热量,通常叫反应热;化学平衡状态的特征:“等”即 V正=V逆>0;“动”即是动态平衡,平衡时反应仍在进行;“定”即反应混合物中各组分百分含量不变;“变”即条件改变,平衡被打破,并在新的条件下建立新的化学平衡;与途径无关,外界条件不变,可逆反应无论是从正反应开始,还是从逆反应开始,都可建立同一平衡状态(等效)即可以解答此题.

 阳光试卷单元测试卷系列答案
阳光试卷单元测试卷系列答案【题目】利用甲烷与水反应制备氢气,因原料廉价产氢率高,具有实用推广价值. 已知:①CH4(g)+H2O(g)CO(g)+3H2(g)△H=+206.2kJmol﹣1
②CO(g)+H2O(g)CO2(g)+H2(g)△H=﹣42.3kJmol﹣1
(1)甲烷和水蒸气生成二氧化碳和氢气的热化学方程式为 .
(2)为了探究反应条件对反应CO(g)+H2O(g)CO2(g)+H2(g)△H=﹣42.3kJmol﹣1的影响,某活动小组设计了三个实验,实验曲线如图所示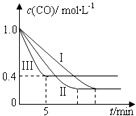
编号 | 温度 | 压强 | c始(CO) | c始(H2O) |
Ⅰ | 530℃ | 3MPa | 1.0molL﹣1 | 3.0molL﹣1 |
Ⅱ | X | Y | 1.0molL﹣1 | 3.0molL﹣1 |
Ⅲ | 630℃ | 5MPa | 1.0molL﹣1 | 3.0molL﹣1 |
①请依据实验曲线图补充完整表格中的实验条件:X=℃,Y=MPa.
②实验Ⅲ从开始至平衡,其平均反应速度率v (CO)=molL﹣1min﹣1 .
③实验Ⅱ达平衡时CO的转化率实验Ⅲ达平衡时CO的转化率(填“大于”、“小于”或“等于”).
④在530℃时,平衡常数K=1,若往10L容器中投入2.0mol CO(g)、2.0mol H2O(g)、1.0mol CO2(g)、1.0mol H2(g),此时化学反应将(填“正向”、“逆向”或“不”) 移动.
【题目】二氧化硫的含量是空气质量监测的一个重要指标.
(1)I.二氧化硫被雨水吸收后就形成了酸雨,某兴趣小组同学汲取热电厂附近的雨水进行实验. ①测得该雨水样品的pH为4.73;
②每隔1h,通过pH计测定雨水样品的pH,测得的结果如表:
测定时间/h | 0 | 1 | 2 | 3 | 4 |
雨水样品的pH | 4.73 | 4.62 | 4.56 | 4.55 | 4.55 |
根据以上信息,回答下列问题:
正常雨水的pH为5.6,偏酸性,这是因为 .
(2)分析上述数据变化,你认为形成这一变化的原因是 .
(3)II.兴趣小组同学为测定空气中二氧化硫的体积分数,做了如下实验:取标准状况下的空气1.000L(内含氮气、氧气、二氧化硫、二氧化碳等),慢慢通过足量氯水,(反应的化学方程式为SO2+Br2+H2O=2HBr+H2SO4),在所得溶液中加入过量的氯化钡溶液,产生白色沉淀,将沉淀洗涤、干燥,称得其质量为0.233g. ①过滤时,除去沉淀中附着的过量氧化钡的方法是 .
②计算该空气样品中二氧化硫的体积分数(写出计算过程)