题目内容
19.上海自主研发了一种氢燃料汽车.它是以30%KOH溶液为电解质的氢氧燃料电池,下列有关说法中,不正确的是( )| A. | 正极反应:O2+2H2O+4e-═4OH- | |
| B. | 当正极消耗22.4 L H2时,负极11.2 L O2消耗(相同条件) | |
| C. | 发生氧化反应的是负极 | |
| D. | 氢氧燃料电池不仅能量转化率高,而且产物是水,属于环境友好电池 |
分析 根据电极反应式知,氢氧燃料碱性电池中,通入氢气的电极是负极,该极上发生氧化反应,通入氧气的电极是正极,该极上是氧气发生得电子的还原反应,电池反应式为2H2+O2=2H2O,燃烧产物是水,环保无污染.
解答 解:A、氢氧燃料碱性电池中,通入氧气的电极是正极,该极上是氧气发生得电子的还原反应,正极反应:O2+2H2O+4e-═4OH-,故A正确;
B、正极反应:O2+2H2O+4e-═4OH-,在正极上消耗的是氧气,负极上消耗的是氢气,故B错误;
C、氢氧燃料碱性电池中,通入氢气的电极是负极,该极上发生氧化反应,故C正确;
D、在燃料电池工作时,化学能大多数转化为电能,能量转化率高,并且2H2+O2=2H2O知,氢氧燃料电池的产物是水,水对环境没有污染,所以属于环境友好电池,故D正确.
故选B.
点评 本题考查原电池的组成以及工作原理,题目难度不大,注意电极反应式以及能量的转换形式,注意燃料电池中燃料不燃烧,为易错点.

练习册系列答案
相关题目
9. 思考下列问题,按要求填空:
思考下列问题,按要求填空:
(1)某温度下纯水中c(H+)=2×10-7mol/L,①此时溶液中的c(OH-)=2×10-7mol/L.
②若温度不变,向水中滴入稀盐酸使c(H+)=5×10-6mol/L,则此时溶液中的c(OH-)=8×10-9mol/L
(2)已知下列热化学方程式:Zn(s)+21 O2(g)═ZnO(s)△H1=-351.1kJ•mol-1;
Hg(l)+21 O2(g)═HgO(s)△H2=-90.7kJ•mol-1
由此可知反应Zn(s)+HgO(s)═ZnO(s)+Hg(l)的焓变为-260.4kJ/mol
(3)在稀氨水中存在下述电离平衡NH3+H2O?NH3•H2O?NH4++OH-,分别加入少量下列物质,溶液中c(OH-)如何变化?(填“增大”、“减小”或“不变”);平衡移动方向如何?(填“正向”、“逆向”或“不移动”)
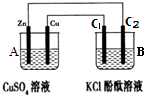
(4)如图所示,装置B中两电极均为石墨电极,试回答下列问题:
①判断装置的名称:A池为原电池.
②锌极为负极,电极反应式为Zn-2e-=Zn2+;
③当C2极析出224mL气体(标准状况下),锌的质量减少_0.65_g.
 思考下列问题,按要求填空:
思考下列问题,按要求填空:(1)某温度下纯水中c(H+)=2×10-7mol/L,①此时溶液中的c(OH-)=2×10-7mol/L.
②若温度不变,向水中滴入稀盐酸使c(H+)=5×10-6mol/L,则此时溶液中的c(OH-)=8×10-9mol/L
(2)已知下列热化学方程式:Zn(s)+21 O2(g)═ZnO(s)△H1=-351.1kJ•mol-1;
Hg(l)+21 O2(g)═HgO(s)△H2=-90.7kJ•mol-1
由此可知反应Zn(s)+HgO(s)═ZnO(s)+Hg(l)的焓变为-260.4kJ/mol
(3)在稀氨水中存在下述电离平衡NH3+H2O?NH3•H2O?NH4++OH-,分别加入少量下列物质,溶液中c(OH-)如何变化?(填“增大”、“减小”或“不变”);平衡移动方向如何?(填“正向”、“逆向”或“不移动”)
| 加入的物质 | 少量(NH4)2SO4固体 | 少量HNO3溶液 | 少量KOH溶液 |
| c(OH-)的变化 | 减小 | 减小 | 增大 |
| 平衡移动方向 | 逆向 | 正向 | 逆向 |
①判断装置的名称:A池为原电池.
②锌极为负极,电极反应式为Zn-2e-=Zn2+;
③当C2极析出224mL气体(标准状况下),锌的质量减少_0.65_g.
10.某铜矿石中铜元素含量较低,且含有铁、镁、钙等杂质离子.某小组在实验室中用浸出-萃取法制备硫酸铜:

(1)操作II、操作III的主要目的是除去杂质、富集铜元素.
(2)小组成员利用CuSO4溶液与Na2CO3溶液混合反应,制备环保型木材防腐剂 Cu2(0H)2C03悬浊液.多次实验发现所得蓝色悬浊液颜色略有差异,查阅资料表明,可能由于条件控制不同使其中混有较多Cu(OH)2或Cu4(0H)6S04.已知Cu(0H)2、Cu2(OH)2CO3、Cu4(0H)6S04均难溶于水,可溶于酸;分解温度依次为80℃、200℃、300℃,设计实验检验悬浊液成分,完成表中内容.
限选试剂:2mol.L-1 HCl、1mol.L-1 H2SO4、O.1mol.L-1 NaOH、0.1mol.L-1 BaCl2、蒸馏水.仪器和用品自选.

(1)操作II、操作III的主要目的是除去杂质、富集铜元素.
(2)小组成员利用CuSO4溶液与Na2CO3溶液混合反应,制备环保型木材防腐剂 Cu2(0H)2C03悬浊液.多次实验发现所得蓝色悬浊液颜色略有差异,查阅资料表明,可能由于条件控制不同使其中混有较多Cu(OH)2或Cu4(0H)6S04.已知Cu(0H)2、Cu2(OH)2CO3、Cu4(0H)6S04均难溶于水,可溶于酸;分解温度依次为80℃、200℃、300℃,设计实验检验悬浊液成分,完成表中内容.
限选试剂:2mol.L-1 HCl、1mol.L-1 H2SO4、O.1mol.L-1 NaOH、0.1mol.L-1 BaCl2、蒸馏水.仪器和用品自选.
| 实验步骤 | 预期现象和结论 |
| 步骤1:取少量悬浊液,过滤,充分洗涤后,取滤渣于试管中,加入过量2mol.L-1HCl,充分振荡,再加0.1mol.L-1BaCl2溶液 | 说明悬浊液中混有白色沉淀产生,有Cu4(0H)6S04. |
| 步骤2:另取少量悬浊液于试管中将试管放入装有沸水的小烧杯中,用水浴加热一段时间,取出试管观察 | 试管中黑色沉淀生成,说明悬浊液中混有Cu(0H)2. |
7.某离子化合物的晶体中,最小重复单元及其八分之一结构单元如图所示,具有该晶体结构的化合物可能是( )


| A. | CaF2 | B. | CO2 | C. | NaCl | D. | CsCl |
14.下列各分子中所有原子都满足最外层为8电子稳定结构的化合物是( )
| A. | BeCl2 | B. | PCl3 | C. | PCl5 | D. | N2 |
4.下列可构成原电池装置的是( )
| A. |  | B. | 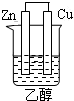 | C. |  | D. | 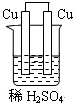 |
11.下列各组离子在水溶液中能够大量共存的是( )
| A. | Ba2+、SO42-、SO32- | B. | Na+、C1-、OH- | ||
| C. | NH4+、OH -、SO42- | D. | H+、CO32-、NO3- |
8.设NA表示阿伏加德罗常数,下列叙述中正确的是( )
| A. | 1molSiO2晶体内含有2NA个Si-O键 | |
| B. | 在0.1mol熔融KHSO4中,含有0.1NA个SO42- | |
| C. | 在0.5L 1mol•L-1的盐酸中所含粒子总数为NA | |
| D. | 1molSi晶体内含有2NA个Si-Si键 |