题目内容
10. 纯过氧化氢是淡蓝色的黏稠液体,可任意比例与水混合,是一种强氧化剂,水溶液俗称双氧水,为无色透明液体.其水溶液适用于医用伤口消毒及环境消毒和食品消毒.
纯过氧化氢是淡蓝色的黏稠液体,可任意比例与水混合,是一种强氧化剂,水溶液俗称双氧水,为无色透明液体.其水溶液适用于医用伤口消毒及环境消毒和食品消毒.(1)请写出H2O2的电子式
 .
.(2)往硫酸中加入一定浓度的双氧水可将溶解铜,写出该反应的离子方程式Cu+H2O2+2H+=Cu2++2H2O.
(3)Fe3+催化H2O2分解的机理可分两步反应进行,第一步反应为:2Fe3++H2O2═2Fe2++O2↑+2H+,请完成第二步反应的离子方程式:□Fe2++□H2O2+□2H+═□2 Fe3+,+□2H2O
(4)如图是一种用电解原理来制备过氧化氢并用产生的H2O2处理废氨水的装置
①为了不影响H2O2的产量,需要向废氨水加入适量硝酸调节溶液的pH约为5,则所得废氨水溶液中c(NH4+)<c(NO3-)(填“>”、“<”或“=”).
②Ir-Ru惰性电极有吸附O2作用,该电极上的反应为O2+2H++2e-═H2O2.
③理论上电路中每转移3mol电子,最多可以处理NH3•H2O的物质的量为1mol.
分析 (1)双氧水中两个氢原子分别与两个氧原子通过共用一对电子结合,两个氧原子之间通过共用1对电子结合;
(2)铜和硫酸在双氧水的作用下发生反应生成硫酸铜和水;
(3)总反应为2H2O2═2H2O+O2↑,第一步反应为2Fe3++H2O2═2Fe2++O2↑+2H+,则总反应减去第一步反应为第二步反应的方程式;
(4)①根据溶液呈电中性,溶液中阳离子所带的正电荷总数等于溶液中阴离子所带的负电荷总数进行解答;
②在该电解池中,Ir-Ru惰性电极有吸附O2作用为氧气得电子发生还原反应,在酸性条件下生成过氧化氢;
③根据4NH3+3O2?2N2+6H2O,每转移12mol电子,处理4mol氨气,据此分析解答.
解答 解:(1)双氧水为共价化合物,分子中存在两个氧氢键和一个O-O键,双氧水的电子式为: ,故答案为:
,故答案为: ;
;
(2)铜和硫酸在双氧水的作用下发生反应生成硫酸铜和水,即Cu+H2O2+2H+=Cu2++2H2O,
故答案为:Cu+H2O2+2H+=Cu2++2H2O;
(3)总反应为2H2O2═2H2O+O2↑,第一步反应为2Fe3++H2O2═2Fe2++O2↑+2H+,则总反应减去第一步反应为第二步反应2Fe2++H2O2+2H+═2Fe3++2H2O,
故答案为:2,1,2H+,2 Fe3+,2H2O;
(4)①向废氨水加入适量硝酸调节溶液的pH约为5,根据溶液呈电中性,溶液中c(NH4+)+c(H+)=c(NO3-)+c(OH-),pH约为5呈酸性,c(H+)>c(OH-),所以c(NH4+)<c(NO3-),故答案为:<;
②利用电解法制H2O2,在该电解池中,Ir-Ru惰性电极有吸附O2作用为氧气得电子发生还原反应,O2+2H++2e-═H2O2,故答案为:O2+2H++2e-═H2O2;
③4NH3+3O2?2N2+6H2O中,氨气中的氮元素从-3价变为氮气中的0价,4mol氨气转移12mol电子,所以转移3mol电子,最多可以处理NH3•H2O的物质的量为1mol,
故答案为:1mol.
点评 本题考查了离子浓度大小比较、电极反应式、电子式的书写以及氧化还原反应中据电子守恒的计算,题目难度中等.

| A. | 碳酸氢钠溶液与少量石灰水反应:HCO3+Ca2++OH-=CaCO3↓+H2O | |
| B. | 次氯酸钙溶液中通入过量二氧化碳:Ca2++2ClO+H20+CO2=CaCO3↓+2HClO | |
| C. | 向NaHSO4溶液中逐滴加入Ba(OH)2溶液至中性:Ba2++2OH+2H++SO42-=BaSO4↓+2H2O | |
| D. | 碳酸氢钙溶液中加入盐酸:HCO3+H+=CO2↑+H20 |
| A. | A原子的最外层电子数比B原子的最外层电子数少 | |
| B. | B的最高价氧化物水化物的碱性强于A的最高价氧化物水化物的碱性 | |
| C. | 1molA与酸反应生成的H2比1molB与酸反应生成的H2多 | |
| D. | 常温时,A能从水中置换出氢气,而B不能 |
①
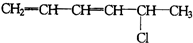
②
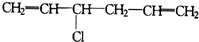
③

④
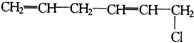
⑤
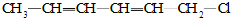
| A. | ③④⑤不可能有 | B. | 只有⑤不可能有 | C. | 全部可能有 | D. | 只有②不可能有 |
| A. | 硝酸见光分解 | B. | 硝酸银溶液与盐酸反应 | ||
| C. | 钢铁生锈 | D. | 白薯发酵制白酒 |
| A. | Na2CO3晶体 | B. | NaOH晶体 | C. | CuSO4溶液 | D. | CH3COONa晶体 |
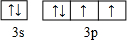 .
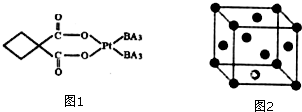
.
 图甲池和乙池中的四个电极都是惰性材料,乙池溶液分层,下层为四氯化碳,上层溶液为盐溶液,呈中性,请根据图示回答下列问题:
图甲池和乙池中的四个电极都是惰性材料,乙池溶液分层,下层为四氯化碳,上层溶液为盐溶液,呈中性,请根据图示回答下列问题: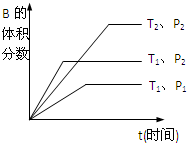 (1)已知某可逆反应mA(g)+nB(g)?qC(g)在密闭容器中进行.如图所示反应在不同时间t,温度T和压强P与反应物B的体积分数的关系曲线.根据图象填空
(1)已知某可逆反应mA(g)+nB(g)?qC(g)在密闭容器中进行.如图所示反应在不同时间t,温度T和压强P与反应物B的体积分数的关系曲线.根据图象填空