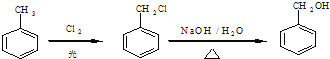
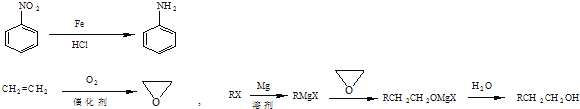题目内容
【题目】铍铜是广泛应用于制造高级弹性元件的良好合金。某科研小组从某废旧铍铜元件(主要含BeO、CuS,还含少量FeS和SiO2)中回收铍和铜两种金属的工艺流程如下:
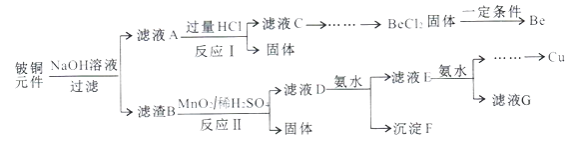
已知:i.铍、铝元素化学性质相似;BeCl2熔融时能微弱电离。
ii.常温下:Ksp[Cu(OH)2]=2.2×10-20, Ksp[Fe(OH)3]=4.0×10-38,Ksp[Mn(OH)2]=2.1×10-13。
回答下列问题:
(1)滤液A的主要成分除NaOH外,还有___________(填化学式);写出反应I中含铍化合物与过量盐酸反应的离子方程式:___________。
(2)滤液C中含NaCl、BeCl2和少量HCl,为得到较纯净的BeCl2溶液,选择下列实验操作最合理步骤的顺序是___________;电解熔融BeCl2制备金属铍时,需要加入NaCl,其作用是___________。
①加入过量的NaOH:②加入过量的氨水;③加入适量的HCl;④过滤;⑤洗涤。
(3)反应Ⅱ中CuS的氧化产物为S单质,该反应的化学方程式为___________。
(4)常温下,若滤液D中c(Cu2+)=2.2mol·L-1、c(Fe3+)=0.008mol·L-1、c(Mn2+)=0.21mol·L-1,向其中逐滴加入稀氨水,生成沉淀F是________(填化学式);为了尽可能多的回收铜,所得滤液G的pH最大值为___________。
【答案】Na2SiO3、Na2BeO2; BeO22-+4H+=Be2++2H2O; ②④⑤③; 增强熔融盐的导电性; MnO2+CuS+2H2SO4=S+MnSO4+CuSO4+2H2O; Fe(OH)3; 8.0;
【解析】
Be、Al元素化学性质相似,废旧铍铜元件中加入NaOH溶液,BeO、SiO2反应转化成Na2BeO2、Na2SiO3进入滤液A中,滤渣B中含CuS、FeS;滤液A中加入过量HCl,Na2SiO3反应生成H2SiO3沉淀和NaCl,Na2BeO2与过量HCl反应生成NaCl、BeCl2和H2O,滤液C中含HCl、NaCl、BeCl2;MnO2具有氧化性,滤渣B中加入MnO2和H2SO4,CuS、FeS反应生成CuSO4、Fe2(SO4)3、S,MnO2被还原为MnSO4;滤液D中主要含CuSO4、Fe2(SO4)3、MnSO4,根据题给Cu(OH)2、Fe(OH)3、Mn(OH)2的溶度积,滤液D中加入氨水得到的沉淀F为Fe(OH)3;滤液E中加入氨水调节pH使Cu2+与Mn2+分离。据此分析作答。
Be、Al元素化学性质相似,废旧铍铜元件中加入NaOH溶液,BeO、SiO2反应转化成Na2BeO2、Na2SiO3进入滤液A中,滤渣B中含CuS、FeS;滤液A中加入过量HCl,Na2SiO3反应生成H2SiO3沉淀和NaCl,Na2BeO2与过量HCl反应生成NaCl、BeCl2和H2O,滤液C中含HCl、NaCl、BeCl2;MnO2具有氧化性,滤渣B中加入MnO2和H2SO4,CuS、FeS反应生成CuSO4、Fe2(SO4)3、S,MnO2被还原为MnSO4;滤液D中主要含CuSO4、Fe2(SO4)3、MnSO4,根据题给Cu(OH)2、Fe(OH)3、Mn(OH)2的溶度积,滤液D中加入氨水得到的沉淀F为Fe(OH)3;滤液E中加入氨水调节pH使Cu2+与Mn2+分离。
(1)废旧铍铜元件的成分BeO、CuS、FeS、SiO2,根据信息i,BeO属于两性氧化物,SiO2属于酸性氧化物,能与氢氧化钠溶液反应,反应方程式为BeO+2NaOH=Na2BeO2+H2O、SiO2+2NaOH=Na2SiO3+H2O,CuS、FeS不与氢氧化钠反应,因此滤液A中主要成分是NaOH、Na2SiO3、Na2BeO2;根据信息i,反应I中为Na2BeO2与过量盐酸反应,反应的离子方程式为BeO22-+4H+=Be2++2H2O;
(2)Be、铝元素化学性质相似,先向滤液C中先加入过量的氨水,生成Be(OH)2沉淀,然后过滤、洗涤,再加入适量的HCl,生成BeCl2,合理步骤是②④⑤③;BeCl2熔融时能微弱电离,熔融BeCl2中离子浓度较小,电解熔融BeCl2制备金属铍时,需要加入NaCl,其作用是增大离子浓度,增强熔融盐的导电性;
(3)反应II中CuS中S转化为S单质,MnO2中Mn被还原为Mn2+,根据化合价升降法进行配平,其化学反应方程式为MnO2+CuS+2H2SO4=S+MnSO4+CuSO4+2H2O;