题目内容
【题目】[化学——选修5:有机化学基础](15分)
氟他胺G是一种可用于治疗肿瘤的药物。实验室由芳香烃A制备G的合成路线如下:
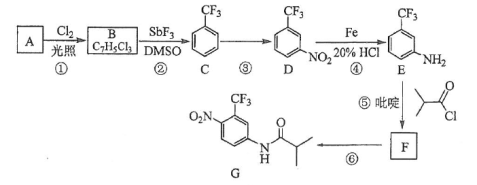
回答下列问题:
(1)A的结构简式为____________。C的化学名称是______________。
(2)③的反应试剂和反应条件分别是____________________,该反应的类型是__________。
(3)⑤的反应方程式为_______________。吡啶是一种有机碱,其作用是____________。
(4)G的分子式为______________。
(5)H是G的同分异构体,其苯环上的取代基与G的相同但位置不同,则H可能的结构有______种。
(6)4-甲氧基乙酰苯胺(![]() )是重要的精细化工中间体,写出由苯甲醚(
)是重要的精细化工中间体,写出由苯甲醚(![]() )制备4-甲氧基乙酰苯胺的合成路线___________(其他试剂任选)。
)制备4-甲氧基乙酰苯胺的合成路线___________(其他试剂任选)。
【答案】
(1)![]() ,三氟甲苯;(2)浓硝酸、浓硫酸,并加热 取代反应;(3)
,三氟甲苯;(2)浓硝酸、浓硫酸,并加热 取代反应;(3)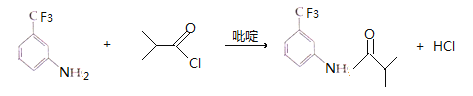
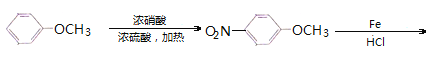
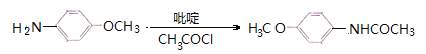
吸收反应产物的HCl,提高反应转化率 (4)C11H11O3N2F3 (5)9种 (6)
【解析】
(1)反应①发生取代反应,应取代苯环取代基上的氢原子,根据B的结构简式,A为甲苯,即结构简式为:![]() ,C的化学名称为三氟甲苯;
,C的化学名称为三氟甲苯;
(2)反应③是C上引入-NO2,且在对位,C与浓硝酸、浓硫酸,并且加热得到,此反应类型为取代反应;(3)根据G的结构简式,反应⑤发生取代反应,Cl取代氨基上的氢原子,即反应方程式为: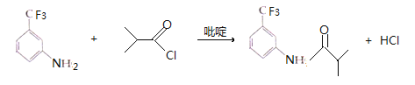 ;吡啶的作用是吸收反应产物的HCl,提高反应转化率;
;吡啶的作用是吸收反应产物的HCl,提高反应转化率;
(4)根据有机物成键特点,G的分子式为:C11H11O3N2F3;
(5)-CF3和-NO2处于邻位,另一个取代基在苯环上有3种位置,-CF3和-NO2处于间位,另一取代基在苯环上有4种位置,-CF3和-NO2属于对位,另一个取代基在苯环上有2种位置,因此共有9种结构;
(6)根据目标产物和流程图,苯甲醚应首先与混酸反应,在对位上引入硝基,然后在铁和HCl作用下-NO2转化成-NH2,最后在吡啶作用下与CH3COCl反应生成目标产物,合成路线是:


 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案