题目内容
下列各溶液中,物质的量浓度关系正确的是
| A.0.1 mol?L—1的KAl(SO4)2溶液中:c(SO42—)>c(K+)>c(A13+)>c(H+)>c(OH—) |
| B.10mL0.01mo1?L—1HCl溶液与10mL0.01mo1?L—1Ba(OH)2溶液充分混合,若混合后溶液的体积为20mL,则溶液的pH=12 |
| C.在01mo1?L—1CH3COONa溶液中,c(OH—)=c(CH3COOH)+c(H+) |
| D.等体积、等物质的量浓度的NaX和弱酸HX混合后的溶液,若溶液呈酸性,则有c(Na+)>c(HX)>c(X—)>c(H+)>c(OH—) |
AC
解析试题分析:A、根据电离方程式、盐类水解、强弱电解质的电离可知,正确;B、酸碱中和时碱过量,则c(OH—)= =5×10—3mol?L—1,c(H+)=
=5×10—3mol?L—1,c(H+)=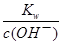 =2×10—12mol?L—1,pH<12,错误;H2O
=2×10—12mol?L—1,pH<12,错误;H2O H++OH—,水电离出的部分H+与CH3COO—结合生成CH3COOH,由质子守恒原理可知,正确;D、违反电荷守恒原理,HX的电离程度大于NaX的水解程度,由物料守恒原理可知,c(X—)>c(Na+)>c(HX)>c(H+)>c(OH—),错误。
H++OH—,水电离出的部分H+与CH3COO—结合生成CH3COOH,由质子守恒原理可知,正确;D、违反电荷守恒原理,HX的电离程度大于NaX的水解程度,由物料守恒原理可知,c(X—)>c(Na+)>c(HX)>c(H+)>c(OH—),错误。
考点:考查水溶液中的粒子浓度大小比较等相关知识。

练习册系列答案
相关题目
下列能正确表示水解的离子方程式是
A.CH3COOH + H2O  CH3COO- + H3O+ CH3COO- + H3O+ |
B.Br- + H2O  HBr + OH- HBr + OH- |
C.CO32- + 2H2O H2CO3 + 2OH- H2CO3 + 2OH- |
D.NH4+ + H2O  NH3·H2O + H+ NH3·H2O + H+ |
下列溶液中各微粒的浓度关系正确的是
| A.pH=4的盐酸中:c(H+)=4.0mol·L-1 |
| B.NH4Cl溶液中:c(Cl-)=c(NH4+) |
| C.NaCl溶液中:c(Na+) + c(H+)= c(Cl-)+c(OH-) |
| D.NaHCO3溶液中:c(HCO3-)+c(H2CO3)+ c(CO32-) =c(Na+) |
向ZnSO4溶液中加入Na2S溶液时,得到白色沉淀,然后向白色沉淀中滴加CuSO4溶液,发现沉淀变为黑色,则下列说法不正确的是
| A.白色沉淀为ZnS,黑色沉淀为CuS |
| B.利用该原理可实现一种沉淀转化为更难溶的沉淀 |
| C.上述现象说明ZnS的Ksp小于CuS的Ksp |
| D.该过程破坏了ZnS的溶解平衡 |
下列溶液中有关微粒的物质的量浓度关系正确的是
| A.在醋酸钠溶液中:c(CH3COOH) = c(OH-) - c(H+) |
| B.等体积等物质的量浓度的NaCl和NaClO溶液中离子总数:N前<N后 |
| C.1mol?L-1的(NH4)2Fe(SO4)2?6H2O溶液中:c(NH4+)=c(SO42-)>c(Fe2+)>c(H+) |
| D.0.1 mol?L-1NaHX溶液pH=3,则此溶液中:c(HX-)>c(H2X)>c(X2-) |
某温度下,向一定体积的0.1mol/L醋酸溶液中逐滴加入0.1mol/LNaOH溶液,溶液中pOH【注:pOH=-lgc(OH-)】与pH的变化关系如图所示,则下列说法中正确的是
| A.M点所示溶液中c(Na+)﹥c(CH3COO-)﹥c(OH-)﹥c(H+) |
| B.N点所示溶液中c(CH3COO-)﹥c(Na+) |
| C.M点和N点所示溶液中水的电离程度相同 |
| D.Q点消耗NaOH溶液的体积等于醋酸溶液的体积 |
20℃时,有体积相同的四种溶液:①pH=3的CH3COOH溶液 ②pH=3的盐酸 ③pH=11的氨水 ④pH=11的NaOH溶液。下列说法不正确的是
| A.若将四种溶液稀释100倍,溶液pH的大小顺序:③>④>①>② |
| B.③和④分别用等浓度的硫酸溶液中和,消耗硫酸溶液的体积:③>④ |
| C.①与②混合,所得混合溶液的pH=3 |
| D.②和③混合后,溶液呈碱性 |
下列叙述或表示正确的是( )
| A.常温下pH均为3的醋酸和硫酸的水溶液,分别加水稀释100倍后,两种溶液的pH仍相同 |
| B.氢氧化钙溶液中加入过量的碳酸氢钙溶液的离子方程式:Ca2+ + HCO3—+OH— = CaCO3 ↓+ H2O |
| C.Ksp反映了难熔电解质在水中的溶解能力,它的大小与浓度无关,与温度无关。 |
| D.c(H+)=1×10-2 mol·L的溶液:Fe2+、Ba2+、N03-、Cl-不能大量共存。 |