题目内容
已知下热化学方程式:
①H2(g)+1/2O2(g)= H2O(l) ⊿H1= —285.8 kJ/mol
②H2(g)+1/2O2(g)= H2O(g) ⊿H2= —241.8kJ/mol
③C(s)+1/2O2 (g) =" CO" (g) ⊿H3= —110.5kJ/mol
④C(s)+ O2 (g) = CO2 (g) ⊿H4= —393.5kJ/mol
回答下列问题:
(1)比较⊿H1, ⊿H2,⊿H3, ⊿H4的大小
(2)上述反应中属于放热的是
(3)H2的燃烧热为 ,C的燃烧热为
(4)燃烧10g H2生成液态水,放出的热量为
(5)CO的燃烧热为 ,其热化学方程式为
(6)分别燃烧1mol C,H2,CO;充分燃烧后它们放出的热量分别为Q1,Q2,Q3
试比较Q1,Q2,Q3的大小
①H2(g)+1/2O2(g)= H2O(l) ⊿H1= —285.8 kJ/mol
②H2(g)+1/2O2(g)= H2O(g) ⊿H2= —241.8kJ/mol
③C(s)+1/2O2 (g) =" CO" (g) ⊿H3= —110.5kJ/mol
④C(s)+ O2 (g) = CO2 (g) ⊿H4= —393.5kJ/mol
回答下列问题:
(1)比较⊿H1, ⊿H2,⊿H3, ⊿H4的大小
(2)上述反应中属于放热的是
(3)H2的燃烧热为 ,C的燃烧热为
(4)燃烧10g H2生成液态水,放出的热量为
(5)CO的燃烧热为 ,其热化学方程式为
(6)分别燃烧1mol C,H2,CO;充分燃烧后它们放出的热量分别为Q1,Q2,Q3
试比较Q1,Q2,Q3的大小
(1) ⊿H3 >⊿H2, , >⊿H1, >⊿H4 。
(2) ①②③④ 。
(3)⊿H= —285.8 kJ/mol或285.8 kJ/mol
⊿H= —393.5kJ/mol或393.5kJ/mol
(4) 1429 kJ
(5) 283kJ/mol或⊿H=" —283" kJ/mol
CO (g) +1 /2O2 (g) = CO2 (g) ⊿H=" —283" kJ/mol
(6) Q1>Q2>Q3
(2) ①②③④ 。
(3)⊿H= —285.8 kJ/mol或285.8 kJ/mol
⊿H= —393.5kJ/mol或393.5kJ/mol
(4) 1429 kJ
(5) 283kJ/mol或⊿H=" —283" kJ/mol
CO (g) +1 /2O2 (g) = CO2 (g) ⊿H=" —283" kJ/mol
(6) Q1>Q2>Q3
略

练习册系列答案
 时刻准备着暑假作业原子能出版社系列答案
时刻准备着暑假作业原子能出版社系列答案 暑假衔接教材期末暑假预习武汉出版社系列答案
暑假衔接教材期末暑假预习武汉出版社系列答案 假期作业暑假成长乐园新疆青少年出版社系列答案
假期作业暑假成长乐园新疆青少年出版社系列答案
相关题目
 4NO (g)+ 6H2O(g)
4NO (g)+ 6H2O(g)
 2NO(g),是导致汽车尾气中含有NO的原因之一。T ℃时,向容积为2 L的密闭容器中充入10 mol N2与5 mol O2,达到平衡后NO的物质的量为2 mol,则T ℃时该反应的平衡常数K= ▲ 。(计算结果保留小数点后两位数字)
2NO(g),是导致汽车尾气中含有NO的原因之一。T ℃时,向容积为2 L的密闭容器中充入10 mol N2与5 mol O2,达到平衡后NO的物质的量为2 mol,则T ℃时该反应的平衡常数K= ▲ 。(计算结果保留小数点后两位数字) 

 N2吸
N2吸 +
+ (某温度下其离子积常数为10-30)。液氨中的pNH4与水中的pH相似,则该温度下液氨的pNH4=_________________。
(某温度下其离子积常数为10-30)。液氨中的pNH4与水中的pH相似,则该温度下液氨的pNH4=_________________。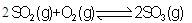
 (Q>0),若向一密闭容器中加入1molSO2和0.5molO2充分反应后,放出的热量为0.5QkJ
(Q>0),若向一密闭容器中加入1molSO2和0.5molO2充分反应后,放出的热量为0.5QkJ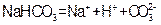

 、
、 时,
时, 完全燃烧生成气态水,放出
完全燃烧生成气态水,放出 热量,则氢气的燃烧热为241.8
热量,则氢气的燃烧热为241.8