题目内容
17.下列相关的叙述中正确的是( )| A. | 生成物的总能量一定低于反应物总能量 | |
| B. | 吸热反应一定要加热才能进行 | |
| C. | 天然气属于可再生能源和一次能源 | |
| D. | 太阳能的开发利用有助于降低碳排放量 |
分析 A、化学反应过程中一定伴随能量变化,反应可以是放热反应或吸热反应;
B、反应放热还是吸热与反应条件无关,决定于反应物和生成物的能量高低;
C、天然气属于不可再生能源和一次能源;
D、太阳能属于清洁能源,对环境无污染.
解答 解:A、化学反应过程中一定伴随能量变化,反应可以是放热反应或吸热反应,反应物能量可以高于生成物反应放热,反应物能量低于生成物,反应吸热反应,故A错误;
B、氯化铵与氢氧化钡反应吸热但不需要任何条件,故B错误;
C、天然气属于不可再生能源和一次能源,故C错误;
D、太阳能属于清洁能源,对环境无污染,大力开发利用太阳能,减小化石燃料的使用,可降低碳排放量,故D正确;
故选:D.
点评 本题考查了化学反应能量变化的分析判断,新能源和化石能源,掌握基础是关键,题目较简单.

练习册系列答案
相关题目
7.Al(OH)3溶度积Ksp为1.6×-33,则0.2mol•L-1AlCl3溶液不产生沉淀的最大OH-物质的量浓度(mol•L)为( )
| A. | 1.9×-33 | B. | 2.0×10-11 | C. | 8.0×10-33 | D. | 2.5×10-5 |
8.还原沉淀法是处理含铬(Cr2O72-和CrO42-)废水常用方法,过程如下:
CrO42-$\stackrel{H+}{→}$Cr2O72-$\stackrel{Fe_{2}+}{→}$Cr3+$\stackrel{OH-}{→}$Cr(OH)3
已知废水中Cr的含量为26.0g•L-1,当溶液中离子浓度小于10-5mol/L时认为离子已经沉淀完全,常温下,Ksp[Cr(OH)3]=1×10-32.有关叙述中不正确的是( )
CrO42-$\stackrel{H+}{→}$Cr2O72-$\stackrel{Fe_{2}+}{→}$Cr3+$\stackrel{OH-}{→}$Cr(OH)3
已知废水中Cr的含量为26.0g•L-1,当溶液中离子浓度小于10-5mol/L时认为离子已经沉淀完全,常温下,Ksp[Cr(OH)3]=1×10-32.有关叙述中不正确的是( )
| A. | 上述三个转化中只有一个涉及氧化还原反应 | |
| B. | 第二步离子方程式为:Cr2O72-+14H++6Fe2+=2Cr3++7H2O+6Fe3+ | |
| C. | 处理含铬废水可使用强碱Ba(OH)2,也可以使用弱碱氨水 | |
| D. | 当pH≥5时,废水中铬元素沉淀完全 |
5.下列有关化学用语正确的是( )
| A. | 乙醛的结构简式为CH3COH | B. | 乙烷的结构简式为:CH3CH3 | ||
| C. | 羟基的电子式为[:O:H]- | D. | 氯离子的结构示意图为: |
2.图为铁、铜水果电池(酸性)装置示意图,下列说法正确的是( )
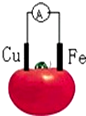

| A. | 铜片为负极 | B. | 铁片上发生还原反应 | ||
| C. | 电流由铁片沿导线流向铜极 | D. | 铜片上的电极方程式:2H++2e-=H2↑ |
9.提出元素周期律并绘制了第一张元素周期表的化学家是( )
| A. | 道尔顿 | B. | 侯德榜 | C. | 拉瓦锡 | D. | 门捷列夫 |
6.一定条件下,反应A+2B=2C,若用物质B表示的速率是1mol/(L?s),则相同条件下用物质A表示的速率是( )
| A. | 1mol/(L?s) | B. | 2mol/(L?min) | C. | 2mol/(L?s) | D. | 0.5mol/(L?s) |
7.丙烯酸(CH2=CH-COOH)的性质可能有( )
①取代反应;②加成反应;③氧化反应;④酯化反应;⑤水解反应.
①取代反应;②加成反应;③氧化反应;④酯化反应;⑤水解反应.
| A. | ①、②、③、④ | B. | ②、③、④、⑤ | C. | ①、②、④、⑤ | D. | 全部 |

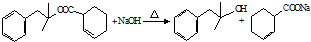 .
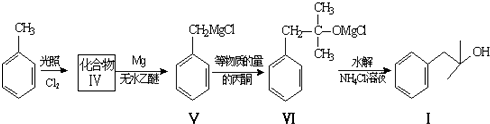
.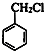 ,生成化合物Ⅳ的反应类型为取代反应.
,生成化合物Ⅳ的反应类型为取代反应.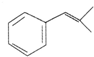 或
或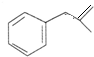 .
. 也能发生类似Ⅴ→Ⅵ的反应生成化合物Ⅶ,则Ⅶ的结构简式为
也能发生类似Ⅴ→Ⅵ的反应生成化合物Ⅶ,则Ⅶ的结构简式为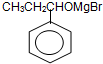 .
.