题目内容
(12分)有A 、B 、C 、D四种元素,A元素形成的-2价阴离子比氦原子的核外电子数多8个,B 元素的一种氧化物为淡黄色固体,该固体遇到空气能生成A的单质,C为原子核内有12个中子的二价金属,当2 .4克C与足量热水反应时,在标准状况下放出气体2.24L ,D的M层上7个电子。
(1)写出A的原子结构示意图: 。B的离子结构示意图:
(2)分别写出B 、D的最高价氧化物的水化物的化学式______,_______.
(3)用电子式表示B与D形成的化合物的过程:
(4)C与D两元素最高价氧化物的水化物反应的离子方程式
(1)写出A的原子结构示意图: 。B的离子结构示意图:
(2)分别写出B 、D的最高价氧化物的水化物的化学式______,_______.
(3)用电子式表示B与D形成的化合物的过程:
(4)C与D两元素最高价氧化物的水化物反应的离子方程式
(12分)(1)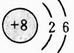
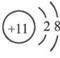 (2)NaOH, HClO4
(2)NaOH, HClO4
(3)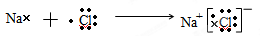
(4)Mg(OH)2+2H+=Mg2++2H2O
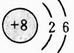
 (2)NaOH, HClO4
(2)NaOH, HClO4 (3)
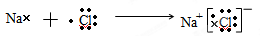
(4)Mg(OH)2+2H+=Mg2++2H2O
A元素形成的-2价阴离子比氦原子的核外电子数多8个,所以A是O。B 元素的一种氧化物为淡黄色固体,该固体遇到空气能生成A的单质,则B是Na,最高价是+1价,所以最高价氧化物的水化物的化学式为NaOH。2.24L氢气是0.1mol,转移电子是0.2mol。所以C的相对原子质量是24,则C是Mg。D的M层上7个电子,因此D是Cl,最高价是+7价,所以最高价氧化物的水化物的化学式为HClO4。钠和氯形成的氯化钠是含有离子键的离子化合物,其形成过程为
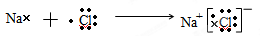 。
。
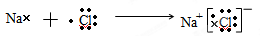 。
。
练习册系列答案
相关题目