题目内容
【题目】已知2A(g) ![]() B(g)+2C(g)为放热反应,下列有关说法错误的是( )
B(g)+2C(g)为放热反应,下列有关说法错误的是( )
A. 该反应属于可逆反应B. A可以完全转化为B和C
C. 化学变化伴随能量变化D. 2molA比2molC的总能量高
【答案】B
【解析】
已知该反应为放热反应,则反应物的总能量大于生成物的总能量;由方程式用可逆号表示可知该反应为可逆反应,据此解答。
A. 由方程式用可逆号表示可知该反应为可逆反应,A项正确;
B. 该反应为可逆反应,则A不能完全转化为B和C,B项错误;
C. 任何化学变化都伴随着能量变化,C项正确;
D. 该反应为放热反应,反应物的总能量大于生成物的总能量,则2molA比2molC和1molB的总能量高,可知2molA比2molC的总能量高,D项正确;
答案选B。

练习册系列答案
相关题目
【题目】下图所示的装置中,烧瓶中充满干燥气体a,然后打开弹簧夹f,将滴管中的液体b挤入烧瓶内,轻轻振荡烧瓶,烧瓶中的液体d呈喷泉喷出,最终几乎充满烧瓶。下列各组不可能出现上述现象的是
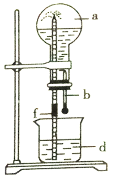
序号 | a(干燥气体) | b(液体)与d(液体) |
A | NO | 水 |
B | CO2 | 4mol·L-1NaOH溶液 |
C | Cl2 | 4mol·L-1NaOH溶液 |
D | NH3 | 1mol·L-1盐酸 |
A.AB.BC.CD.D