题目内容
15.下列实验方案合理的是( )| A. | 用溴水或酸性KMnO4溶液鉴别甲烷和乙烯 | |
| B. | 向酒精中加入足量生石灰检验酒精中是否含有少量水 | |
| C. | 在盛有2mL无水乙醇的试管中放入绕成螺旋状的光洁铜丝,加热可制得乙醛 | |
| D. | 将裂解气通入到酸性KMnO4溶液中来证明裂解气中是否有乙烯 |
分析 A.乙烯能使溴水或酸性高锰酸钾溶液褪色,但甲烷和溴水或酸性高锰酸钾溶液都不反应;
B.水能使无水硫酸铜变蓝色,所以可以用无水硫酸铜检验水;
C.在Cu作催化剂、加热条件下,乙醇被氧化生成乙醛;
D.烯烃能被酸性高锰酸钾溶液氧化而使酸性高锰酸钾溶液褪色.
解答 解:A.乙烯和溴发生加成反应生成1,2-二溴乙烷而使溴水褪色,乙烯被酸性高锰酸钾溶液氧化生成二氧化碳而使酸性高锰酸钾溶液褪色,但甲烷和溴水或酸性高锰酸钾溶液都不反应,所以可以用溴水或酸性高锰酸钾溶液鉴别甲烷和乙烯,故A正确;
B.水能使无水硫酸铜变蓝色,所以可以用无水硫酸铜检验水,但可以用足量生石灰除去酒精中的水分,故B错误;
C.加热变黑生成CuO,再与乙醇发生氧化反应,重复几次,完成乙醇氧化为乙醛的实验,故C错误;
D.烯烃能被酸性高锰酸钾溶液氧化而使酸性高锰酸钾溶液褪色,将裂解气通入到酸性KMnO4溶液中来证明裂解气中是否有烯烃而不是乙烯,故D错误;
故选A.
点评 本题考查化学实验方案评价,为高频考点,侧重考查物质鉴别、除杂、基本操作等知识点,明确物质性质及性质差异性是解本题关键,注意从实验操作的规范性、实验评价性分析,题目难度不大.

练习册系列答案
相关题目
5.某无色透明的溶液能够与铝作用生成氢气,则在此溶液中一定能大量共存的离子组是( )
| A. | HCO3-、NO3-、Ba2+、Cl- | B. | Na+、Ba2+、Cl-、NO3- | ||
| C. | K+、NH4+、Cl-、OH- | D. | Na+、K+、SO42-、I- |
6.将一定质量的铁投入20mL浓硫酸中,加热充分反应后固体有剩余并收集气体4.48L(标准状况),质量为6.6g;则
(1)参加反应的铁的质量为11.2g.
(2)硫酸溶液的物质的量浓度为15mol/L.
(1)参加反应的铁的质量为11.2g.
(2)硫酸溶液的物质的量浓度为15mol/L.
10.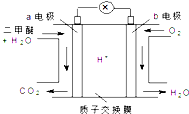 二甲醚(CH3OCH3)是一种绿色、可再生的新能源.下图是绿色电源“燃料电池”的工作原理示意图(a、b均为多孔性Pt电极).该电池工作时,下列说法错误的是( )
二甲醚(CH3OCH3)是一种绿色、可再生的新能源.下图是绿色电源“燃料电池”的工作原理示意图(a、b均为多孔性Pt电极).该电池工作时,下列说法错误的是( )
 二甲醚(CH3OCH3)是一种绿色、可再生的新能源.下图是绿色电源“燃料电池”的工作原理示意图(a、b均为多孔性Pt电极).该电池工作时,下列说法错误的是( )
二甲醚(CH3OCH3)是一种绿色、可再生的新能源.下图是绿色电源“燃料电池”的工作原理示意图(a、b均为多孔性Pt电极).该电池工作时,下列说法错误的是( )| A. | a电极为该电池负极 | |
| B. | O2在b电极上得电子,被氧化 | |
| C. | 电池工作时,a电极反应式:CH3OCH3-12e-+3H2O═2CO2↑+12H+ | |
| D. | 电池工作时,燃料电池内部H+从a电极移向b电极 |
20.用下列实验装置进行相应实验,能达到实验目的是( )
| 选项 | A | B | C | D |
| 装置 | 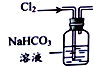 | 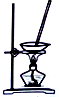 | 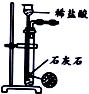 | 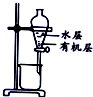 |
| 目的 | 除去Cl2中含有的少量HCl | 蒸发NaCl饱和溶液制备NaCl晶体 | 制取少量纯净的CO2气体 | 分离酒精和水的混合溶液 |
| A. | A | B. | B | C. | C | D. | D |
7.下列关于离子化合物的叙述不正确的是( )
| A. | 离子化合物中都含有离子键 | |
| B. | 离子化合物中的阳离子只能是金属离子 | |
| C. | 有些离子化合物可能含有共价键 | |
| D. | 溶于水可以导电的化合物一定是离子化合物 |
4.已知蓄电池在放电时起原电池的作用,充电时起电解他的作用.铅蓄电池在放电和充电时发生的化学反应可用下式表示:Pb+PbO2+2H2SO4$?_{充电}^{放电}$2PbSO4+2H2O据此判断下列叙述中正确的是( )
| A. | 在放电时,正极发生的反应是Pb(s)+SO42-(ag)-2e-═PbSO4(s) | |
| B. | 在充电时,电池中硫酸的浓度不断变小 | |
| C. | 在充电时,阴极发生的反应是PbSO4(s)+2e-═Pb(s)+SO42-(ag) | |
| D. | 在放电时,该电池的负极材料是氧化铅 |
5.下列表示对应化学反应或过程的离子方程式正确的是( )
| A. | 铜片插入硝酸银溶液中:Cu+Ag+═Cu2++Ag | |
| B. | 碳酸氢钙与过量的NaOH溶液反应Ca2++2HCO3-+2OH-═CaCO3↓+2H2O+CO32- | |
| C. | 用石墨作电极电解AlCl3溶液:2Cl-+2H2O$\frac{\underline{\;电解\;}}{\;}$ Cl2↑+H2↑+2OH- | |
| D. | FeCl3溶液用于蚀刻印刷电路:Cu+2Fe3+═Cu2++2Fe2+ |