题目内容
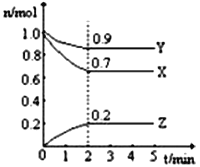
【题目】向容积固定为2L的密闭容器中充入9.6molNO和4.8molO2,发生如下反应:①2NO(g)+O2(g) ![]() 2NO2(g)△H<0 ②2NO2(g)=N2O4(g) 测得NO2和N2O4的浓度变化如图所示,0~10min维持容器温度为T℃,10min时改变某反应条件,一段时间后再次平衡。下列说法正确的是
2NO2(g)△H<0 ②2NO2(g)=N2O4(g) 测得NO2和N2O4的浓度变化如图所示,0~10min维持容器温度为T℃,10min时改变某反应条件,一段时间后再次平衡。下列说法正确的是
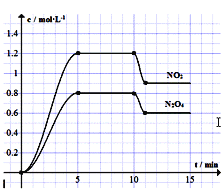
A. 前5min反应的平均速率v(NO)=0.24mol·(L·min)-1
B. T℃时反应①的化学平衡常数K=0.36
C. 10min时改变反应条件可能是降低温度
D. 若起始时向该容器中充入1.6mol NO2和4.0mol N2O4,T℃达到平衡时,NO2的物质的量浓度与图中5~10min的不同
【答案】B
【解析】试题分析:A、反应①中消耗的c(NO)=1.2mol/L+0.8×2mol/L=2.8mol/L,前5min反应的平均速率v(NO2)=△c÷△t=2.8mol/L÷5min=0.56mol(Lmin)-1,故v(NO)=0.56mol(Lmin)-1,A错误;B、应①中消耗的c(NO)=2.8mol/L,消耗的c(O2)=0.5×2.8mol/L=1.4mol/L,因此达到平衡后,c(NO)=9.6mol÷2L-2.8mol/L=2mol/L,c(O2)=4.8mol÷2L-1.4mol/L=1mol/L,c(NO2)=1.2mol/L,则反应①的化学平衡常数K=![]() =0.36,B正确;C,在该题中,反应为放热,降低温度后,平衡正向移动,四氧化二氮的浓度增加,C错误;D、若起始时向该容器中充入1.6mol NO2和4.0mol N2O4,与之前的充入量等效,故NO2的物质的量浓度与图中5~10min的相同,D错误,答案选B。
=0.36,B正确;C,在该题中,反应为放热,降低温度后,平衡正向移动,四氧化二氮的浓度增加,C错误;D、若起始时向该容器中充入1.6mol NO2和4.0mol N2O4,与之前的充入量等效,故NO2的物质的量浓度与图中5~10min的相同,D错误,答案选B。

 口算题卡北京妇女儿童出版社系列答案
口算题卡北京妇女儿童出版社系列答案【题目】在甲、乙、丙三个不同密闭容器中按不同方式投料,一定条件下发生反应(起始温度和起始体积相同):A2(g)+3B2(g)![]() 2AB3(g) ΔH<0,相关数据如下表所示:
2AB3(g) ΔH<0,相关数据如下表所示:
容器 | 甲 | 乙 | 丙 |
相关条件 | 恒温恒容 | 绝热恒容 | 恒温恒压 |
反应物投料 | 1mol A2、3molB2 | 2molAB3 | 2mol AB3 |
反应物的转化率 | a甲 | a乙 | a丙 |
反应的平衡常数K= | K甲 | K乙 | K丙 |
平衡时AB3的浓度/mol·L-1 | c甲 | c乙 | c丙 |
平衡时AB3的反应速率/mol·L-1·min-1 | v甲 | v乙 | v丙 |
下列说法正确的是
A. v甲=v丙 B. c乙< c丙 C. a甲 +a乙<1 D. K乙≤K丙