题目内容
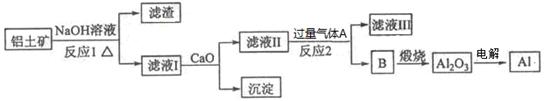
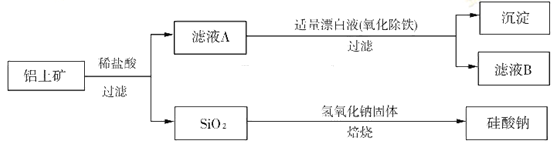
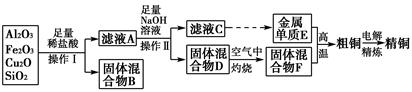
用含有Al2O3及少量Fe2O3和SiO2的铝土矿制备净水剂——液体聚合硫酸铝铁,工艺流程如下(部分操作和条件略):
I.向铝土矿中加入过量H2SO4后,加热、搅拌、过滤。
II.向滤液中加入一定量的FeSO4·7H2O和双氧水。
III.向溶液中加入Ca(OH)2固体,调节溶液的pH约为1,过滤。
IV.加入稳定剂,加热,得到产品。
(1)Fe2O3与H2SO4反应的离子方程式是___________。
(2)步骤I中过滤得到的滤渣成分是________(填化学式)。
(3)步骤I 中H2SO4的浓度与反应温度会影响铁与铝的浸出率。根据下图分析,步骤I 中H2SO4浓度的适宜范围是__________,反应的适宜温度是_________。


(4)步骤II中增大n(Fe3+)的离子方程式是_________。
(5)步骤III得到碱式硫酸铝铁[AlFe(OH)n(SO4)m]的溶液,则步骤II中应增大n(Fe3+)到
n(Al3+)﹕n(Fe3+)= 。
(6)研究表明,液体聚合硫酸铝铁的纯度越高,净水效果越好。已知:
一些物质在20℃时的溶解度
| 物质 | Ca(OH)2 | CaSO4 | Na2SO4 |
| 溶解度/g | 0.153 | 0.258 | 19.5 |
结合表中数据,解释步骤III中使用Ca(OH)2而不用NaOH的原因__________。
(7)铝土矿也可用于冶炼金属Al。以金属Al作阳极,稀硫酸作电解液,通过电解会使金属Al的表面生成致密坚硬的氧化膜,其电极反应式是_________。
(1)Fe2O3+6H+=2Fe3++3H2O(2)SiO2(3)45%~50%;100℃(4)H2O2+2Fe2++2H+=2H2O+2Fe3+(5)1﹕1(6)使用Ca(OH)2,既能调节溶液的pH,又生成溶解度较小的CaSO4,得到的液体聚合硫酸铝铁的纯度较高。(7)2Al-6e—+3H2O =Al2O3+6H+
解析试题分析:(1)硫酸溶解氧化铝生成硫酸铝和水,离子方程式:Al2O3+6H+=2Al3++3H2O;(2)Fe2O3与硫酸反应生成铁离子,Al2O3与硫酸反应生成铝离子,而SiO2不与硫酸发生反应,故过滤后的滤渣为SiO2;(3)由图知,浸出率铁铝最高的硫酸浓度范围为45%~50%;反应适宜温度铁为80℃铝为100℃,故最适宜温度为100℃(4)FeSO4被双氧水在酸性溶液中氧化生成Fe3,H2O2+2Fe2++2H+=2H2O+2Fe3+(5)碱式硫酸铝铁中铝铁的系数相同其物质的量比也应相等,故n(Al3+)﹕n(Fe3+)=1:1(6)氢氧化钠和氢氧化钙都可以调节pH,但氢氧化钠反应生成的硫酸钠溶液水,与生成物碱式硫酸铝铁混合在溶液中不易分离,而硫酸钙溶解度较小,使生成物中杂质较少;(7)阳极Al失电子生成,电极反应式2Al-6e—+3H2O =Al2O3+6H+。
考点:化学反应方程式的书写;铝的重要化合物;铁的氧化物

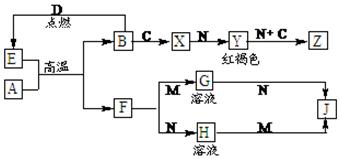
我国从澳大利亚进口的某高炉生铁(用A表示)的成分如下(其余是铁):
| C | Si | Mn | P | S |
| 4.070% | 2.900% | 0.495% | 0.165% | 0.010% |
(2)磷肥的肥效以相当含P2O5多少来表示。炼钢时,P元素形成炉渣Ca3(PO4)2,后者再与浓硫酸反应制得普通过磷酸钙[即普钙,成分是CaSO4、Ca(H2PO4)2和少量其它杂质]。若某普钙中Ca(H2PO4)2的质量分数为45.25%,则含P2O5的质量分数至少是 %。
(3)锰的质量分数为30%的高锰钢有很好的性能,可制作火车车轮。将A冶炼成含碳0.4%、含锰30%的高锰钢(设铁无损耗,其它杂质已除去,可补充锰),则100吨A可制得高锰钢 吨。
(4)某炼钢厂的烟尘成分和质量分数如下表:
| | FeO | Fe2O3 | CaO |
| 烟尘煅烧前(%) | 86.40 | 4.00 | 9.60 |
为了减少烟尘的排放,将烟尘与CO混合后在空气中煅烧,得到铁的氧化物和CaO的烧结物,其中CaO的质量分数为8.92%(金属元素无损耗),烧结物分离出CaO后,若铁的氧化物中只有两种物质组成,则铁的氧化物的组成和物质的量之比如何?
 Fe2O3+SO2↑+SO3↑。
Fe2O3+SO2↑+SO3↑。