题目内容
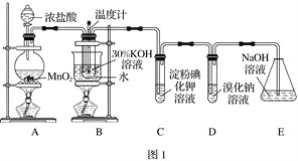
【题目】利用下图装置(夹持装置略)制取和收集纯净、干燥的氨气,并探究氨气的性质。
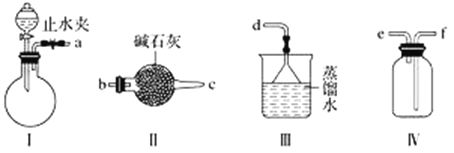
(1)关闭装置Ⅰ中的止水夹,向分液漏斗中加适量水,打开活塞,说明Ⅰ气密性良好的现象是______________________。
(2)利用装置Ⅰ制取氨气,不能选用的试剂为浓氨水和________(填字母)。
A.氢氧化钠 B.碱石灰 C.硝酸钾 D.生石灰
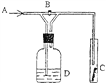
(3)根据实验要求,仪器连接的顺序(用字母编号表示):a接________、________接________、______接______。______
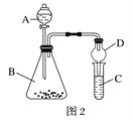
(4)收集氨气,按如图装置进行NH3性质的探究实验。
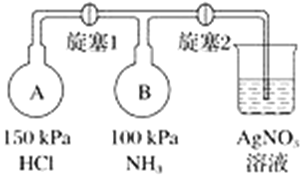
①打开旋塞1,B瓶中的现象是_________________________________________,原因是_____________________________________________,稳定后,关闭旋塞1;
②再打开旋塞2,B瓶中的现象是__________________________________________。
【答案】分液漏斗内液面不再下降 C c b e f d 产生白色的烟 氯化氢与氨气反应生成了氯化铵小颗粒,NH3+HCl=NH4Cl,氯化铵小颗粒形成白烟 烧杯中的硝酸银溶液会倒流进入到B瓶中,B瓶中生成白色沉淀(提示:A中气体压强大于B中)
【解析】
(1)利用注水法检验装置的气密性;
(2)利用装置I制取氨气,为常温下固液制取气体的装置,据此分析;
(3)依据氨气的物质性质和化学性质选择连接方式;
(4)A中压强大,HCl进入B中,与氨气反应生成氯化铵固体;关闭旋塞①,再打开旋塞②,烧杯中的AgNO3溶液会倒流进入到B瓶中,反应生成AgCl。
(1)关闭A装置中的止水夹,向分液漏斗中加入适量水,打开活塞,分液漏斗内液面高度保持不变(或液体不再滴下),说明A装置气密性良好,故答案为:分液漏斗内液面不再下降;
(2)利用装置I制取氨气,为常温下固液制取气体的装置,可为浓氨水与CaO、氢氧化钠,CaO+H2O=Ca(OH)2、消耗水并放热,根据NH3+H2O![]() NH3
NH3![]() H2O
H2O![]() NH4++OH-可知,氢氧化钙、氢氧化钠溶于水电离出氢氧根离子,氢氧根离子浓度增大平衡逆向移动,使氨气逸出,且温度升高,降低氨气的溶解度,使氨气逸出,A、B、D符合条件,硝酸钾溶于水没有明显的热效应,不能与浓氨水制备氨气,故答案为:C;
NH4++OH-可知,氢氧化钙、氢氧化钠溶于水电离出氢氧根离子,氢氧根离子浓度增大平衡逆向移动,使氨气逸出,且温度升高,降低氨气的溶解度,使氨气逸出,A、B、D符合条件,硝酸钾溶于水没有明显的热效应,不能与浓氨水制备氨气,故答案为:C;
(3)利用装置I制取氨气,制出的氨气中含有水蒸气,需进行干燥,选用装置Ⅱ,粗口进,细口出,所以a连接cb;根据氨气的密度小于空气的密度,应为向下排气法收集,所以选择收集装置应为“短进长出”,所以再连接ef,氨气属于极易溶于水,还是大气污染气体,用防倒吸的装置进行尾气吸收连接d,所以连接顺序为cbefd,故答案为:c;b;e;f;d;
(4)A容器压强为150 kPa,B容器压强100 kPa,A容器压强大于B容器,先打开旋塞①,A容器中的氯化氢进入B容器,氨气和氯化氢反应,NH3+HCl=NH4Cl,生成氯化铵固体小颗粒,所以B瓶中的现象是出现白烟,氨气、氯化氢为气体反应生成的氯化铵为固体,压强减小,再打开旋塞②,硝酸银倒吸入B瓶中,氯化铵与硝酸银反应生成白色的氯化银沉淀。故答案为:产生白色的烟;氯化氢与氨气反应生成了氯化铵小颗粒,NH3+HCl=NH4Cl,氯化铵小颗粒形成白烟;烧杯中的硝酸银溶液会倒流进入到B瓶中,B瓶中生成白色沉淀(提示:A中气体压强大于B中)。

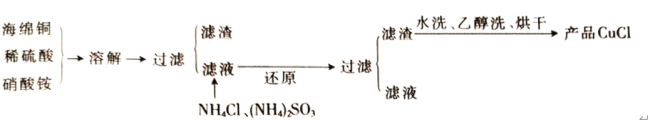
【题目】金属镍在电池和电镀等工业上具有广泛的用途,可镍也具有很强的毒性,若不进行回收处理,将对环境造成很大的影响,以下是以电镀废渣为原料获得NiSO46H2O的过程,已知,废渣中除含金属镍外,主要含有:Cu、Zn、Fe、Mg等元素的化合物。
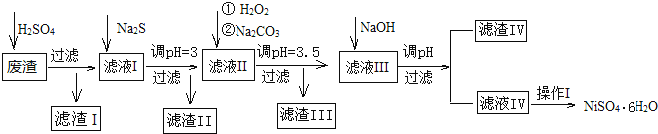
部分阳离子以氢氧化物或硫化物的形式完全沉淀时溶液的pH见表.
沉淀物 | Fe(OH)3 | Fe(OH)2 | CuS | ZnS | FeS | NiS | Al(OH)3 | Mg(OH)2 | Ni(OH)2 |
pH | 3.2 | 9.7 | ≥-0.42 | ≥2.5 | ≥7 | ≥7.5 | ≥5 | ≥8 | ≥8.5 |
(1)往废渣中加H2SO4酸浸,提高酸浸效率的方法有__(至少写出2点)。
(2)加Na2S同时调溶液的pH为3,目的是除去铜、锌等杂质,则往滤液Ⅱ中加入H2O2的反应的离子方程式为___。
(3)操作Ⅰ包括以下过程:__、__、过滤、洗涤、干燥.该洗涤过程不能用水洗涤,应该用__洗涤,目的是___。干燥有低温干燥和高温干燥,能否用高温干燥___,理由是____。
(4)滤液Ⅲ中加入NaOH溶液的目的是调节溶液的pH为8以除去Al3+以及少量的Mg2+,若向含有Mg2+、Al3+的溶液中滴加NaOH溶液,常温下当两种沉淀共存且溶液的pH=8时,c(Mg2+):c(Al3+)=__。{已知:25℃时,Ksp[Mg(OH)2]=5.0×10-14;Ksp[Al(OH)3]=2.0×10-33}。