题目内容
X、Y、Z、W四种化合物均由1~18号元素组成,其中X含有四种元素,X、Y、Z的焰色反应均为黄色,W为无色无味气体.这四种化合物具有下列转化关系如图1(部分反应物、产物及反应条件已略去).请回答:
(1)W的分子式是
(2)X与Y在溶液中反应的离子方程式是
(3)X含有的四种元素之间(二种、三种或四种)可组成多种化合物,选用其中某些化合物,利用图2装置快速制取少量的O2,并演示Na在O2中的燃烧实验.
①关闭装置中的止水夹a后,开启活塞b,漏斗中液体不断地往下滴,直至全部流入试管.试判断装置是否漏气
②写出A装置中反应的化学方程式并标出电子得失情况:
 .
.
③C装置中观察到的现象是
④D装置中盛放的试剂是
(4)向Z溶液中通入氯气,可制得某种生产和生活中常用的漂白、消毒的物质,同时有X生成,该反应的化学方程式是

(1)W的分子式是
CO2
CO2
.(2)X与Y在溶液中反应的离子方程式是
HCO3-+OH-=CO32-+H2O
HCO3-+OH-=CO32-+H2O
.(3)X含有的四种元素之间(二种、三种或四种)可组成多种化合物,选用其中某些化合物,利用图2装置快速制取少量的O2,并演示Na在O2中的燃烧实验.
①关闭装置中的止水夹a后,开启活塞b,漏斗中液体不断地往下滴,直至全部流入试管.试判断装置是否漏气
漏气
漏气
(填“漏气”、“不漏气”或“无法确定”),判断理由是漏斗中的液体能全部流入试管说明试管中压强与外界相同
漏斗中的液体能全部流入试管说明试管中压强与外界相同
.②写出A装置中反应的化学方程式并标出电子得失情况:


③C装置中观察到的现象是
剧烈燃烧,发出黄光,有淡黄色物质生成;
剧烈燃烧,发出黄光,有淡黄色物质生成;
.④D装置中盛放的试剂是
碱石灰
碱石灰
,其作用是防止空气中的H2O、CO2进入C装置
防止空气中的H2O、CO2进入C装置
.(4)向Z溶液中通入氯气,可制得某种生产和生活中常用的漂白、消毒的物质,同时有X生成,该反应的化学方程式是
2Na2CO3+Cl2+H2O=NaClO+NaCl+2NaHCO3
2Na2CO3+Cl2+H2O=NaClO+NaCl+2NaHCO3
.
分析:(1)X、Y、Z、W四种化合物均由1~18号元素组成,其中X含有四种元素,X、Y、Z的焰色反应均为黄色,W为无色无味气体.这四种化合物具有下列转化关系如图1,X、Y、Z的焰色反应均为黄色,说明三者均为钠元素的化合物.X含有四种元素,在加热条件下能生成Z,这四种化合物均为短周期元素组成,且W为无色无味的气体(中学阶段常见的无色无味的气体为H2、O2、CO2等),可推出X为NaHCO3,Y为NaOH,Z为Na2CO3,W为CO2;
(2)X与Y在溶液中反应是NaHCO3+NaOH=Na2CO3+H2O;
(3)X所含的四种元素为:Na、H、C、O,这四种元素组成的化合物有:NaHCO3、Na2CO3、NaOH、H2CO3、Na2O、Na2O2、NaOH、H2O、H2O2、CO2、CO等无机物和烃、烃的含氧衍生物等有机物.选用其中某些化合物,利用图2装置快速制取少量的O2,并演示Na在O2中的燃烧实验.
①依据装置漏气检查的主要依据是装置中的压强关系分析判断;
②依据装置2快速制氧气分析判断A装置是过氧化钠和水反应生成氢氧化钠和氧气的反应;
③依据装置分析,A装置生成氧气干燥后通入加热的金属钠中剧烈反应,钠在氧气中 燃烧生成但黄色固体,火焰呈黄色;
④依据实验目的是验证钠和氧气反应的现象分析;
(4)向Z(Na2CO3)溶液中通入氯气,可制得某种生产和生活中常用的漂白、消毒的物质应为次氯酸钠,同时有X(NaHCO3)生成,依据原子守恒配平写出化学方程式;
(2)X与Y在溶液中反应是NaHCO3+NaOH=Na2CO3+H2O;
(3)X所含的四种元素为:Na、H、C、O,这四种元素组成的化合物有:NaHCO3、Na2CO3、NaOH、H2CO3、Na2O、Na2O2、NaOH、H2O、H2O2、CO2、CO等无机物和烃、烃的含氧衍生物等有机物.选用其中某些化合物,利用图2装置快速制取少量的O2,并演示Na在O2中的燃烧实验.
①依据装置漏气检查的主要依据是装置中的压强关系分析判断;
②依据装置2快速制氧气分析判断A装置是过氧化钠和水反应生成氢氧化钠和氧气的反应;
③依据装置分析,A装置生成氧气干燥后通入加热的金属钠中剧烈反应,钠在氧气中 燃烧生成但黄色固体,火焰呈黄色;
④依据实验目的是验证钠和氧气反应的现象分析;
(4)向Z(Na2CO3)溶液中通入氯气,可制得某种生产和生活中常用的漂白、消毒的物质应为次氯酸钠,同时有X(NaHCO3)生成,依据原子守恒配平写出化学方程式;
解答:解:(1)X、Y、Z的焰色反应均为黄色,说明三者均为钠元素的化合物.X含有四种元素,在加热条件下能生成Z,这四种化合物均为短周期元素组成,且W为无色无味的气体(中学阶段常见的无色无味的气体为H2、O2、CO2等),可推出X为NaHCO3,Y为NaOH,Z为Na2CO3,W为CO2.故答案为:CO2;
(2)X与Y在溶液中反应是NaHCO3+NaOH=Na2CO3+H2O,离子方程式是HCO3-+OH-=CO32-+H2O;故答案为:HCO3-+OH-=CO32-+H2O;
(3)X所含的四种元素为:Na、H、C、O,这四种元素组成的化合物有:NaHCO3、Na2CO3、NaOH、H2CO3、Na2O、Na2O2、NaOH、H2O、H2O2、CO2、CO等无机物和烃、烃的含氧衍生物等有机物;
①关闭装置中的止水夹a后,开启活塞b,漏斗中液体不断地往下滴,直至全部流入试管,说明装置漏气,因为漏斗中的液体能全部流入试管,说明试管中压强与外界相同漏气;
故答案为:漏水;漏斗中的液体能全部流入试管说明试管中压强与外界相同;
②A装置中反应是过氧化钠和水的反应,反应的化学方程式为2Na2O2+2H2O=4NaOH+O2↑反应的电子转移情况用双线桥标出电子得失情况为:
 故答案为:
故答案为: ;
;
③C装置中观察到的现象是难在氧气中 燃烧的实验现象,钠剧烈燃烧,发出黄光,有淡黄色物质生成;故答案为:剧烈燃烧,发出黄光,有淡黄色物质生成;
④为避免空气中的二氧化碳和水蒸气进入C装置与钠反应,影响实验现象的判断,干燥管中应装碱石灰;故答案为:碱石灰; 防止空气中的H2O、CO2进入C装置;
(4)向Z(Na2CO3)溶液中通入氯气,可制得某种生产和生活中常用的漂白、消毒的物质应为次氯酸钠,同时有X(NaHCO3)生成,依据原子守恒配平得到化学方程式为:2Na2CO3+Cl2+H2O=NaClO+NaCl+2NaHCO3;故答案为:2Na2CO3+Cl2+H2O=NaClO+NaCl+2NaHCO3;
(2)X与Y在溶液中反应是NaHCO3+NaOH=Na2CO3+H2O,离子方程式是HCO3-+OH-=CO32-+H2O;故答案为:HCO3-+OH-=CO32-+H2O;
(3)X所含的四种元素为:Na、H、C、O,这四种元素组成的化合物有:NaHCO3、Na2CO3、NaOH、H2CO3、Na2O、Na2O2、NaOH、H2O、H2O2、CO2、CO等无机物和烃、烃的含氧衍生物等有机物;
①关闭装置中的止水夹a后,开启活塞b,漏斗中液体不断地往下滴,直至全部流入试管,说明装置漏气,因为漏斗中的液体能全部流入试管,说明试管中压强与外界相同漏气;
故答案为:漏水;漏斗中的液体能全部流入试管说明试管中压强与外界相同;
②A装置中反应是过氧化钠和水的反应,反应的化学方程式为2Na2O2+2H2O=4NaOH+O2↑反应的电子转移情况用双线桥标出电子得失情况为:
 故答案为:
故答案为: ;
;③C装置中观察到的现象是难在氧气中 燃烧的实验现象,钠剧烈燃烧,发出黄光,有淡黄色物质生成;故答案为:剧烈燃烧,发出黄光,有淡黄色物质生成;
④为避免空气中的二氧化碳和水蒸气进入C装置与钠反应,影响实验现象的判断,干燥管中应装碱石灰;故答案为:碱石灰; 防止空气中的H2O、CO2进入C装置;
(4)向Z(Na2CO3)溶液中通入氯气,可制得某种生产和生活中常用的漂白、消毒的物质应为次氯酸钠,同时有X(NaHCO3)生成,依据原子守恒配平得到化学方程式为:2Na2CO3+Cl2+H2O=NaClO+NaCl+2NaHCO3;故答案为:2Na2CO3+Cl2+H2O=NaClO+NaCl+2NaHCO3;
点评:本题考查了元素化合物的相互转化,实验操作和实验设计的原理应用,是高考出题的热点之一.题目往往以框图推断题的形式展现,纵观近几年的高考试题,会发现这类试题的突破点(题眼)在逐渐减少,难度在逐渐增加.这就要求学生必须对元素化合的知识非常熟练,在学习时要让学生多总结、多联系,形成知识网络.

练习册系列答案
相关题目
 (2011?江苏)原子序数小于36的X、Y、Z、W四种元素,其中X是形成化合物种最多的元素,Y原子基态时最外层电子数是其内层电子数的2倍,Z原子基态时2p原子轨道上有3个未成对的电子,W的原子序数为29.
(2011?江苏)原子序数小于36的X、Y、Z、W四种元素,其中X是形成化合物种最多的元素,Y原子基态时最外层电子数是其内层电子数的2倍,Z原子基态时2p原子轨道上有3个未成对的电子,W的原子序数为29.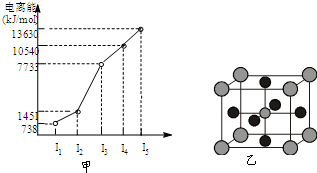 有X、Y、Z、W四种元素,原子序数依次减小.已知X是第四周期的主族元素,其部分电离能如图甲所示;X、Y元素具有相同的最高正化合价;Z 原子p轨道共有3个电子;W原子价电子排布式为nsnnpn.
有X、Y、Z、W四种元素,原子序数依次减小.已知X是第四周期的主族元素,其部分电离能如图甲所示;X、Y元素具有相同的最高正化合价;Z 原子p轨道共有3个电子;W原子价电子排布式为nsnnpn.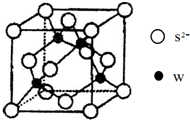 原子序数小于36的X、Y、Z、W四种元素,其中X原子基态时2p原子轨道上有3个未成对电子,Y原子基态时最外层电子数是其内层电子数的3倍,Z元素的最高价氧化物的水化物的酸性最强,W的原子序数为30.
原子序数小于36的X、Y、Z、W四种元素,其中X原子基态时2p原子轨道上有3个未成对电子,Y原子基态时最外层电子数是其内层电子数的3倍,Z元素的最高价氧化物的水化物的酸性最强,W的原子序数为30.