题目内容
【题目】![]() 时,由弱酸
时,由弱酸![]() 及其盐
及其盐![]() 组成的混合溶液,起始浓度均为
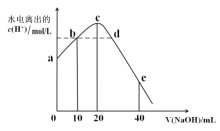
组成的混合溶液,起始浓度均为![]() 。如图为向该溶液中通入HCl气体或加入NaOH固体时,溶液pH随加入
。如图为向该溶液中通入HCl气体或加入NaOH固体时,溶液pH随加入![]() 或
或![]() 的物质的量而变化的曲线。下列说法中,不正确的是
的物质的量而变化的曲线。下列说法中,不正确的是
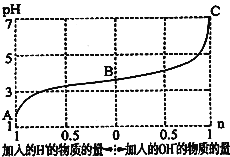
A.A、B、C三点所表示的溶液中水的电离程度依次增大
B.加入1molNaOH后,溶液中![]()
C.通入HCl,![]() 的水解程度增大,HA的电离常数减小
的水解程度增大,HA的电离常数减小
D.未加HCl和NaOH时,溶液中![]()
【答案】C
【解析】
A.A、B溶液呈酸性,抑制水的电离,C呈中性,pH越小,酸性越强,水的电离程度越小,则A、B、C三点所表示的溶液中水的电离程度依次增大,选项A正确;
B.加入1molNaOH后,![]() ,溶液呈中性,即
,溶液呈中性,即![]() ,由电荷守恒可知
,由电荷守恒可知![]() ,选项B正确;
,选项B正确;
C.电离常数只受温度的影响,通入HCl,HA的电离常数不变,选项C错误;
D.未加HCl和NaOH时,溶液呈酸性,说明HA的电离程度大于![]() 水解程度,则
水解程度,则![]() ,选项D正确。
,选项D正确。
答案选C。

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
【题目】某同学用KSCN溶液和![]() 溶液探究
溶液探究![]() 的还原性时出现异常现象,实验如下:
的还原性时出现异常现象,实验如下:
|
|
|
|
|
|
溶液变红,大约10秒左右红色褪去,有气体生成 | 溶液变红且不褪色,有气体生成 | 溶液变红且不褪色,滴加盐酸和 |
下列说法不正确的是
A.对比![]() ,可以判定酸性条件下
,可以判定酸性条件下![]() 可以氧化
可以氧化![]()
B.实验![]() 中发生的氧化还原反应有两种
中发生的氧化还原反应有两种
C.![]() 中红色溶液中含有
中红色溶液中含有![]() 胶体
胶体
D.![]() 中发生的氧化还原反应为:
中发生的氧化还原反应为:![]()