题目内容
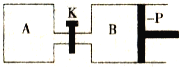
【题目】如图所示的装置中发生反应2A2(g)+B2(g)![]() 2C(g) △H=—a kJ/mol(a>0),已知P是可自由滑动的活塞。在相同温度进关闭K,向A、B容器中分别充入2molA2和1molB2,两容器分别在500℃时达到平衡,A中C的浓度为
2C(g) △H=—a kJ/mol(a>0),已知P是可自由滑动的活塞。在相同温度进关闭K,向A、B容器中分别充入2molA2和1molB2,两容器分别在500℃时达到平衡,A中C的浓度为![]() mol/L,放出热量b kJ,B中C的浓度分别为
mol/L,放出热量b kJ,B中C的浓度分别为![]() mol/L,放出热量c kJ。请回答下列问题:
mol/L,放出热量c kJ。请回答下列问题:
(1)若将温度升高到700℃,反应的平衡常数将_____(填“增大”、“减小”、或“不变”)。
(2)比较大小: ![]() _____
_____![]() (填“>”、“=”、或“<”),a、b、c由大到小的关系为_____。
(填“>”、“=”、或“<”),a、b、c由大到小的关系为_____。
(3)若打开K,一段时间后重新达到平衡,容器B的体积将_____(填“增大”、“减小”、或“不变”)。
(4)若让A、B体积相等且固定P,在B中改充入4 molA2和2 molB2,在500℃时达到平衡后C的浓度为![]() mol/L,则
mol/L,则![]() 、
、![]() 的关系为_____。
的关系为_____。
(5)能说明A中已达到平衡状态的是_____(填序号,有一个或多个选项符合题意)。
a. ![]() (C)=2
(C)=2![]() (B2) b. 容器内气体压强保持不变
(B2) b. 容器内气体压强保持不变
c. 容器中气体的平均相对分子质量不随时间而变化 d. 容器内的气体密度保持不变
(6)使该反应的反应速率增大,且平衡向正反应方向移动的是_____。
a.及时分离出C气体 b. 适当升高温度 c. 增大B2的浓度 d. 选择高效的催化剂
【答案】 减小 ![]()
![]() 减小
减小 ![]() bc c
bc c
【解析】(1)该反应为放热反应,温度升高,平衡左移,反应的平衡常数将减小;正确答案:减小。
(2)A是恒容容器,B是恒压容器,反应2A 2(g)+B2(g)![]() 2C(g)发生后,气体的物质的量之和减小,所以B相当于在A的基础上加压,增大了压强,B容器内的反应向右移动,C的浓度增大,放出的热量增加;正确答案:
2C(g)发生后,气体的物质的量之和减小,所以B相当于在A的基础上加压,增大了压强,B容器内的反应向右移动,C的浓度增大,放出的热量增加;正确答案: ![]() ;
; ![]() 。
。
(3)若打开K,因为B端的压强大于A端的压强,所以B中压强会减小,活塞P会向左移动,故容器B的体积将减小;正确答案:减小。
(4)若让A、B体积相等且固定P,相当于恒温恒容, B中改充入4 molA2和2 molB2,气体总量是A中气体总量的2倍,气体总量按比例增加相当于加压,压强增大会引起平衡右移,所以![]() ;正确答案:
;正确答案: ![]() 。
。
(5)没有标明两种物质的正、逆反应方向,无法判定反应达到平衡状态,a错误;该反应是一个反应前后气体总量发生变化的反应,所以容器内气体压强保持不变,可以判定反应达到平衡状态,b正确; 反应前后气体的总质量不变,反应前后气体的总量发生变化,根据M=m/n,m不变,n变化,当M不变时,反应达到平衡状态;c正确;恒温恒容,气体的总体积不变,反应前后气体的总质量不变,根据密度计算公式ρ=m/V, m不变,V不变,密度始终不变,无法判定反应达到平衡状态,d错误;正确选项bc。
(6)及时分离出C气体,相当于减少浓度,反应速率减慢,a错误;该反应正反应放热,升高温度,反应速率增大,平衡左移,b错误;增大B2的浓度,反应速率增大,平衡右移,c正确;选择高效的催化剂,化学反应速率增大,平衡不移动,d错误;正确选项c。