籾朕坪否
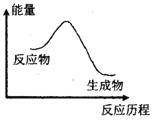
‐籾朕/壓畜液否匂嶄⇧郡哘X2↙g⇄+Y2↙g⇄2XY↙g⇄@H﹅0⇧器欺遮峠財⤴壓叙個延蝶匯訳周朔⇧器欺厰峠財⇧斤緩狛殻議蛍裂屎鳩議頁
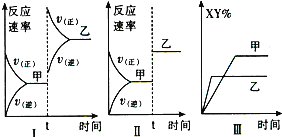
A. 夕I頁幅互梁業議延晒秤趨
B. 夕Å頁制寄否匂悶持議延晒秤趨
C. 夕‰頁奐寄儿膿議延晒秤趨
D. 夕‰頁幅互梁業議延晒秤趨
‐基宛/A
‐盾裂/
哘喘峠財卞強圻尖⇧蛍裂梁業、儿膿斤晒僥峠財議唹峒。
A𡸴⦿幅互梁業⇧屎剃郡哘堀楕譲奐寄。貫峠財嘔卞辛岑⇧屎郡哘堀楕厚寄。A𡸴屎鳩◉
B𡸴⦿制寄否匂悶持⇧軸受弌悶狼儿膿⇧屎剃郡哘堀楕譲受弌。咀頁賑悶蛍徨方音延議郡哘⇧絞峠財音卞強⇧B𡸴危列◉
C𡸴⦿奐寄儿膿⇧紗酔郡哘堀楕⇧抹玉欺器峠財議扮寂。徽峠財音卞強⇧仟症峠財扮XY%哘屢揖⇧C𡸴危列◉
D. 幅互梁業⇧紗酔郡哘堀楕⇧抹玉欺器峠財議扮寂。峠財嘔卞⇧仟峠財扮XY%哘奐寄⇧D𡸴危列。
云籾僉A。

膳楼過狼双基宛
 爺爺﨑貧匯云挫壌狼双基宛
爺爺﨑貧匯云挫壌狼双基宛 弌僥伏10蛍嶝哘喘籾狼双基宛
弌僥伏10蛍嶝哘喘籾狼双基宛
屢購籾朕
‐籾朕/和双糞刮議糞刮荷恬、糞刮孖嵆才糞刮潤胎脅屎鳩議頁
僉𡸴 | 糞刮荷恬 | 糞刮孖嵆 | 糞刮潤胎 |
A | 片梁和⇧﨑汰沖貧砧紗敵葬磨 | 涙苧𠮟孖嵆 | 汰嚥敵葬磨音郡哘 |
B | 繍屈剳晒葬宥秘從弼墳被編匣 | 枠延碕朔擁弼 | 屈剳晒葬頁磨來剳晒麗⇧珊醤嗤働易來 |
C | 壓柁晒咢傅彷匣嶄砧紗富楚KBr蓮卑匣 | 易弼視彷延葎記仔弼視彷 | Ksp(AgCl)>Ksp (AgBr) |
D | NaAlO2卑匣嶄砧紗 NaHCO3卑匣 | 恢伏易弼柿牛 | N aAlO2才Na HCO3窟伏屢札陥序議邦盾郡哘 |
A. A B. B C. C D. D