题目内容
【题目】用下图中的简易装置可以进行气体的发生和收集。
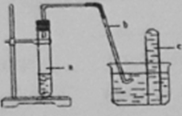
(1)实验前应如何检查该装置的气密性?
(2)拨开试管a的橡皮塞,加入10ml6mol·L-1稀HNO3和1g薄铜片,立即将带有导管的橡皮塞塞紧试管口,反应开始时速度缓慢,逐渐加快,请写出试管a中所发生的所有反应的方程式。
(3)从反应开始到反应结束,预期试管a中可观察到哪些现象?请依次逐一写出。
(4)在反应开始时,可观察到导管b中的水面先沿导管b慢慢上升到一定高度,此后又回落,然后有气泡从管口冒出。试说明反应开始时,导管中水面先上升的原因。
(5)试管c收集满气体后,用拇指堵住管口,取出水槽,将管口向上,松开拇指,片刻后,再次堵住管口,将试管又再倒置于水槽中,松开拇指,此时可观察到什么现象?
【答案】(1)把导管b的下端浸入水中,用手紧握捂热试管a,导管中会有气泡冒出,松手后,水又会回升到导管b中。
(2)①3Cu+8HNO3(稀)=3Cu(NO3)2+2NO↑+4H2O ②2NO+O2=2NO2 ③3NO2+H2O=2HNO3+NO
(3)①铜片和稀HNO3反应,有无色气泡产生,开始缓慢后来加快
②试管上部气体由无色变为浅棕色,又变为无色
③试管a中的溶液由无色变为浅蓝色
④反应结束后,铜片全部消耗完
(4)由于反应开始时产生的NO和试管a上部空气中的O2作用生成NO2,而NO2又易溶于水并与水反应,使装置内气体的压强暂时减小,所以导管中的水面会先上升到一定高度,此后又落回。等到试管上部空气中的O2消耗完以后,NO就会从管口冒出
(5)松开拇指后NO与空气中的氧气反应:2NO+O2=2NO2,3NO2+H2O=2HNO3+NO,导致气体体积减小,液面上升,试管内气体又变为无色
【解析】
试题分析:(1)由该装置图可知,采用“微热法”检验气密性,步骤为:把导管b的下端浸入水中,用手握住试管a,若b导管口处有气泡冒出,放手后在导管b中形成一段水柱,则证明装置气密性良好;
(2)Cu和稀硝酸反应生成硝酸铜、NO和水,NO易被氧气氧化生成二氧化氮,二氧化氮溶于水生成硝酸和NO,所以涉及的反应方程式为3Cu+8HNO3(稀)=3Cu(NO3)2+2NO↑+4H2O、2NO+O2=2NO2、3NO2+H2O=2HNO3+NO;
(3)由发生的反应3Cu+8HNO3(稀)=3Cu(NO3)2+2NO↑+4H2O、2NO+O2=2NO2、可知,铜片逐渐变小直至消失,溶液中有无色气泡产生,该气体在试管上部变为红棕色,试管中的溶液由无色变为浅蓝色;
(4)由于反应开始时产生的NO和试管a上部空气中的O2作用生成NO2,而NO2又易溶于水并与水反应,使装置内气体的压强暂时减小,所以导管中的水面会先上升到一定高度,此后又落回。等到试管上部空气中的O2消耗完以后,NO就会从管口冒出;
(4)松开拇指后NO与空气中的氧气反应:2NO+O2=2NO2,而生成NO2,再投入水中时发生反应:3NO2+H2O=2HNO3+NO,导致气体体积减小,液面上升,试管内气体又变为无色。